
将下列气体通入水中,其饱和水溶液酸性最强的是
| A.CH4 | B.NH3 | C.HBr | D.SO2 |
科目:高中化学 来源: 题型:单选题
20 ℃时H2S饱和溶液1 L,其浓度为0.1 mol·L-1,已知其电离方程式为H2S H++HS-,HS-
H++HS-,HS- H++S2-,若要使该溶液H+及S2-浓度都减小,可采取的措施是
H++S2-,若要使该溶液H+及S2-浓度都减小,可采取的措施是
| A.通入适量的HCl | B.加入适量的NaOH固体 |
| C.通入适量的SO2 | D.加入适量的CuSO4固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某课外实验小组设计的下列实验合理的是 ( )
| A | B | C | D |
 | 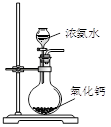 |  |  |
| 装置能验证AgCl沉淀可转化为溶解度更小的Ag2S沉淀 | 制备少量氨气 | 制备并收集少量NO2气体 | 制备少量氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列事实可证明氨水中的(NH3?H2O)是弱碱的是
| A.氨水能被弱酸醋酸中和 | B.铵盐受热易分解 |
| C.氨水可以使酚酞试液变红 | D.常温下,0.1 mol/L氯化铵溶液的pH约为5 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
关于溶液的酸碱性说法正确的是 ( )
| A.c(H+)很小的溶液一定呈碱性 |
| B.PH=7的溶液一定呈中性 |
| C.不能使酚酞试液变红的溶液一定呈酸性 |
| D.c(OH-)= C(H+)的溶液一定呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述中正确的是
| A.常温下,0.01mol·L-1醋酸溶液pH=2 |
| B.95℃纯水的pH<7,说明加热可导致水呈酸性 |
| C.常温下,将pH=3的醋酸溶液稀释至10倍后溶液pH=4 |
| D.常温下,将0.2 mol·L-1的盐酸与等体积水混合后溶液pH=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
A.向 溶液通入 溶液通入 ,可使水解平衡: ,可使水解平衡: 向正反应方向移动,则溶液pH增大 向正反应方向移动,则溶液pH增大 |
B.室温时,0.1mol 某一元酸HA在水中有0.1%发生电离,则该溶液的pH=4 某一元酸HA在水中有0.1%发生电离,则该溶液的pH=4 |
C.25℃时,pH=13的1.0 L Ba  溶液中含有的 溶液中含有的 |
| D.用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列对沉淀溶解平衡的描述正确的是
A.Ksp(AB2)小于Ksp(CD),则AB2的溶解度小于CD的溶解度
B.沉淀溶解达到平衡时,沉淀的速率和溶解的速率相等
C.在氯化银的沉淀溶解平衡体系中,加入蒸馏水,氯化银的Ksp增大
D.沉淀溶解达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,将NaHY晶体加入水中溶解,得到0.1 mol/L NaHY溶液,下列叙述正确的是( )
| A.若NaHY溶液的pH=4,该溶液中粒子浓度关系为:c(Na+)>c(HY-)>c(H+)>c(Y2-)>c(H2Y) |
| B.若NaHY的水溶液显碱性,该溶液中粒子浓度关系为:c(Na+)>c(OH-)>c(H+)>c(HY-) |
| C.若溶液中粒子浓度关系为c(H+)+c(H2Y)=c(OH-)+c(Y2-),则NaHY的水溶液一定显碱性 |
| D.将NaHY晶体加入水中一定能促进水的电离 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com