
【题目】某课外实验小组设计的下列实验不合理的是( )
A. 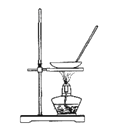 蒸干NH4Cl饱和溶液制备NH4Cl晶体
蒸干NH4Cl饱和溶液制备NH4Cl晶体
B. 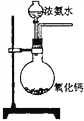 实验室制备少量氨气
实验室制备少量氨气
C. 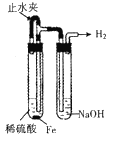 制备并观察氢氧化亚铁
制备并观察氢氧化亚铁
D. 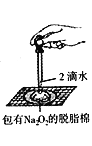 证明过氧化钠与水反应放热
证明过氧化钠与水反应放热
【答案】A
【解析】A.NH4Cl受热易分解,应采用冷却热NH4Cl饱和溶液制备NH4Cl晶体,选项A错误;B.氧化钙与水反应放出热量,使一水合氨发生分解反应生成氨气,可用于实验室制备少量氨气,选项B正确;C.在左边的试管中首先发生Fe+H2SO4 =FeSO4 +H2↑,产生的氢气通过导气管进入到右边的试管中把NaOH溶液中的空气赶走,然后关闭止水夹,这时左边的FeSO4 溶液在氢气的压强下被压入到右边的试管中发生反应:FeSO4 +2NaOH=Na2SO4 +Fe(OH)2↓,由于氢氧化亚铁沉淀处于氢气的环境中,不能被空气氧化,所以可较长时间观察氢氧化亚铁的沉淀,选项C正确;D.2Na2O2 +2H2O=4NaOH+O2↑,如果反应放热,放出的热量能使棉花燃烧起来,可用于证明过氧化钠与水反应放热,选项D正确;答案选A。


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】碳酸钠是一种重要的化工原料,主要采用氨碱法生产。回答下列问题:
(1)碳酸钠俗称 , 可作为碱使用的原因是(用离子方程式表示)。
(2)已知:①2NaOH(s)+CO2(g) ![]() Na2CO3(s)+H2O(g) ΔH1=127.4 kJ·mol1 ②NaOH(s)+CO2(g)
Na2CO3(s)+H2O(g) ΔH1=127.4 kJ·mol1 ②NaOH(s)+CO2(g) ![]() NaHCO3(s) ΔH1=131.5 kJ·mol1
NaHCO3(s) ΔH1=131.5 kJ·mol1
反应2Na2CO3(s) ![]() Na2CO3(s)+ H2O(g) +CO2(g)的ΔH= kJ·mol1 , 该反应的平衡常数表达式K=。
Na2CO3(s)+ H2O(g) +CO2(g)的ΔH= kJ·mol1 , 该反应的平衡常数表达式K=。
(3)向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时溶液中 ![]() =。已知Ksp(BaCO3)=2.6×109 , Ksp(BaSO4)=1.1×1010。
=。已知Ksp(BaCO3)=2.6×109 , Ksp(BaSO4)=1.1×1010。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)Si(g)+4HCl(g);△H=+Q kJmol﹣1(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1mol,则达平衡时,吸收热量为Q kJ
C.反应至4min时,若HCl浓度为0.24 mol/L,则H2的反应速率为0.03 mol/(Lmin)
D.当反应吸收热量为0.025Q kJ时,生成的HCl通入100mL 1molL﹣1的NaOH溶液恰好反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中曲线为一定压强下NO的平衡转化率与温度的关系,图中a、b、c、d四点表示不同温度、压强下2NO(g)+O2(g)2NO2(g)达到平衡时NO的转化率,则压强最大的点为( ) 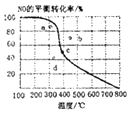
A.a
B.b
C.c
D.d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y和W为原子序数依次递增的短周期元素,X和Y同主族,Y和W 的气态氢化物具有相同的电子数,X元素可以组成M和N两种气态单质,反应 M + 2I-+ 2H+= I2 + N + H2O 常作为 M 的鉴定反应。
(1)M与N的关系为_____________________
(2)写出实验室制取W2的离子方程式____________________________ 。
(3)成外高一某化学兴趣小组设计下图所示的实验装置(图中夹持和加热装置略去),分别探究 YX2和W2 的性质。

①分别通入 YX2 和 W2 时,在装置 A 中观察到的现象是否相同?__________(填“相同”或“不相同”)。
若装置 D 中装的是铁粉,当通入 W2 时观察到的现象为_______________________________________; 若装置 D 中装的是五氧化二钒(V2O5),当通入 YX2 时,打开 K 放入适量的氧气,在 D 装置中发生反应的化学方程式为___________________________________________。
②若装置 B 中装有 5.0 mL 1.0×10-3 mol/L 的碘水,当通入足量W2完全反应后,转移了5.0×10-5mol电子,该反应的化学方程式为_______________________________
(4)某同学将足量的 YX2 通入一支装有 BaCl2 溶液的试管,未见沉淀生成,向该试管中加入适量(填字母) ___________,可以看到白色沉淀产生。
A.氨水 B.稀盐酸C.稀硝酸 D.CaCl2 溶液
(5)若Y和X组成的负二价阴离子Z,Z中Y和X的质量比为 Y∶X = 4∶3,当 W2 与含Z的溶液完全反应后,有黄色沉淀生成,取上层淸液加入 BaCl2 溶液,有白色沉淀产生,该反应的离子方程式为______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是 ( )
A. 18gD2O含有电子数为10NA
B. 46g NO2和N2O4的混合物中所含氮原子个数为6.02×10![]()
C. 0.1mol过氧化钠与足量的水反应,转移的电子数为 0.2NA
D. 50 mL 12 mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[选修3—物质结构与性质]
(1)Ⅰ、下列物质的结构或性质与氢键无关的是( )
A.乙醚的沸点
B.乙醇在水中的溶解度
C.氢化镁的晶格能
D.DNA的双螺旋结构
(2)Ⅱ、钒(23V)是我国的丰产元素,广泛用于催化及钢铁工业。
回答下列问题:
(1)钒在元素周期表中的位置为 ,其价层电子排布图为 。
(2) 钒的某种氧化物的晶胞结构如图1所示。晶胞中实际拥有的阴、阳离子个数分别为 。
(3)V2O5常用作SO2转化为SO3的催化剂。SO2分子中S原子价层电子对数是 对,分子的立体构型为 ;SO3气态为单分子,该分子中S原子的杂化轨道类型为 ;SO3的三聚体环状结构如图2所示,该结构中S原子的杂化轨道类型为 ;该结构中S—O键长由两类,一类键长约140pm,另一类键长约为160pm,较短的键为 (填图2中字母),该分子中含有 个σ键。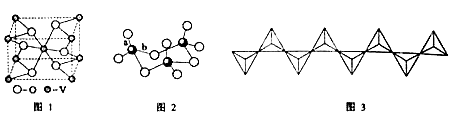
(4) V2O5溶解在NaOH溶液中,可得到钒酸钠(Na2VO4),该盐阴离子的立体构型为 ;也可以得到偏钒酸钠,其阴离子呈如图3所示的无限链状结构,则偏钒酸钠的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素,它们在周期表中位置如图所示,下列说法不正确的是( ) 
A.Z、Y、X的原子半径依次减小,非金属性依次降低
B.Z、Y、W的最高价氧化物对应水化物的酸性依次降低
C.WH4与Z元素的单质在一定条件下可能发生化学反应
D.W的位置是第2周期、第ⅣA族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com