
| A. | 容器内压强不随时间变化 | |
| B. | 容器内各物质的浓度不随时间变化 | |
| C. | 容器内X、Y、Z浓度之比为1:2:2 | |
| D. | 混合气的平均摩尔质量不随时间变化时 |
分析 一定条件下,可逆反应X(g)+2Y(g)?2Z(g)为气体体积缩小的反应,该反应达到平衡状态时,正逆反应速率相等,各组分的浓度、百分含量不再变化,据此进行判断.
解答 解:A.该反应前后气体体积不相等,反应过程中压强为变量,当容器内压强不变时,说明达到平衡状态,故A不选;
B.容器内各物质的浓度不随时间变化,说明正逆反应速率相等,达到了平衡状态,故B不选;
C.X、Y、Z浓度之比为1:2:2,无法判断各组分的浓度是否发生变化,则无法判断是否达到平衡状态,故C选;
D.气体质量始终不变,反应过程中气体的总物质的量为变量,当混合气体的平均摩尔质量不变时,说明达到平衡状态,故D不选;
故选C.
点评 本题考查了化学平衡状态的判断,题目难度不大,明确化学平衡状态的概念、特征及判断方法为解答关键,注意判断平衡状态时必须根据变量的变化情况,试题有利于培养学生的分析、理解能力及灵活应用能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ①④ | C. | ②③ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Br+Br→Br-Br | B. | H-F→H+F | C. | H2+Cl2→HCl | D. | Cs(金刚石)→Cs(石墨) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 原子序数依次增大的A、B、C、D、E、F六种元素.其中A的基态原子有3个不同能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E,F和C位于同一主族,F处于第一个长周期.
原子序数依次增大的A、B、C、D、E、F六种元素.其中A的基态原子有3个不同能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E,F和C位于同一主族,F处于第一个长周期.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 滤液A中的阳离子为Fe2+、Fe3+、H+ | B. | 样品中Fe元素的质量为2.24 g | ||
| C. | 样品中CuO的质量为4.0 g | D. | V=896 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
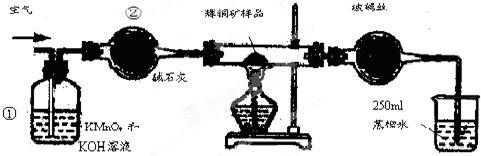
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.04 | 21.03 |
| 2 | 25.00 | 1.98 | 21.99 |
| 3 | 25.00 | 3.20 | 21.24 |
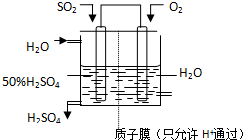
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
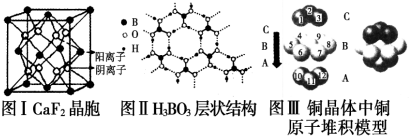
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:H2CO3>HNO3 | B. | 碱性:NaOH>KOH | ||
| C. | 非金属性:Si>P | D. | 气态氢化物稳定性:H2O>H2S |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com