
·ÖĪö ·ÖĄėKClŗĶBaCl2Į½ÖÖ¹ĢĢå»ģŗĻĪļ£¬ĻČČÜÓŚĖ®£¬Č»ŗó¼ÓČė¹żĮæK2CO3Ź¹BaCl2×Ŗ»ÆĪŖ³Įµķ£¬ŌņŹŌ¼ĮaĪŖK2CO3£¬¹żĀĖŗó³Įµķ¼ÓČėŃĪĖįæÉÉś³ÉBaCl2ČÜŅŗŌņŹŌ¼ĮbĪŖŃĪĖį£¬¾Õō·¢”¢½į¾§”¢øÉŌļŗóæÉµĆ¹ĢĢåBaCl2£¬²Ł×÷¢ŚĖłµĆĀĖŅŗĪŖKClŗĶK2CO3µÄ»ģŗĻĪļ£¬Ó¦¼ÓČė¹żĮæŃĪĖįæɵĆKCl£¬ŅŌ“Ė½ā“šøĆĢā£®
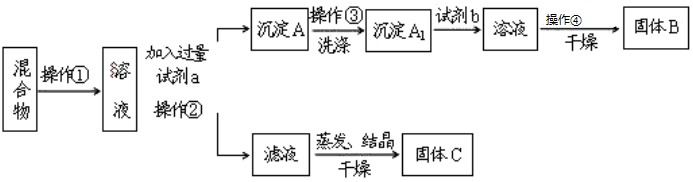
½ā“š ½ā£ŗ£Ø1£©²Ł×÷¢ŚĪŖ¹ĢĢåŗĶŅŗĢåµÄ·ÖĄė£¬ĪŖ¹żĀĖ²Ł×÷£¬²Ł×÷¢ÜÓÉČÜŅŗµĆµ½¾§Ģ壬ĪŖÕō·¢½į¾§£¬¹Ź“š°øĪŖ£ŗ¹żĀĖ£»Õō·¢½į¾§£»
£Ø2£©¹ĢĢåČܽāŗó¼ÓČė¹żĮæK2CO3Ź¹BaCl2×Ŗ»ÆĪŖ³Įµķ£¬¹żĀĖŗó³Įµķ¼ÓČėŃĪĖįæÉÉś³ÉBaCl2ČÜŅŗ£¬¾Õō·¢”¢½į¾§”¢øÉŌļŗóæÉµĆ¹ĢĢåBaCl2£¬
¹Ź“š°øĪŖ£ŗK2CO3£»HCl£»BaCl2£»
£Ø3£©²Ł×÷¢ŪĪŖ³ĮµķµÄĻ“µÓ£¬ŅŌ³żČ„±ķĆęĪüø½µÄŌÓÖŹ£¬·½·ØŹĒĻņ¹żĀĖĘ÷ÖŠ¼ÓĖ®ÖĮøĒ×”¹ĢĢ壬“żĖ®Ā©Ķź£¬ÖŲø“ÉĻŹö²Ł×÷2-3“Ī£¬
¹Ź“š°øĪŖ£ŗĻņ¹żĀĖĘ÷ÖŠ¼ÓĖ®ÖĮøĒ×”¹ĢĢ壬“żĖ®Ā©Ķź£¬ÖŲø“ÉĻŹö²Ł×÷2-3“Ī£»
£Ø4£©¼ÓČėŹŌ¼Įb£¬BaCO3³Įµķ¼ÓČėŃĪĖįæÉÉś³ÉBaCl2ČÜŅŗ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖBaCO3+HCl=BaCl2+CO2”ü+H2O£¬
¹Ź“š°øĪŖ£ŗBaCO3+HCl=BaCl2+CO2”ü+H2O£»
£Ø5£©Õō·¢½į¾§Ē°Ó¦¼ÓČėŹŹĮæĻ”ŃĪĖį£¬½«¹żĮæµÄĢ¼Ėį¼Ų×Ŗ»Æ³ÉĀČ»Æ¼Ų£¬·ńŌņ¾§Ģå²»“棬ĖłŅŌøĆ·½°ø²»·ń“ļµ½ŹµŃéÄæµÄ£¬
¹Ź“š°øĪŖ£ŗ²»ÄÜ£»Ļņ²Ł×÷¢ŚĖłµĆĀĖŅŗÖŠ¼ÓČė×ćĮæµÄHClŗó£¬Õō·¢½į¾§µĆµ½KCl£»
£Ø6£©¹ĢĢåČܽāŗó¼ÓČė¹żĮæK2CO3Ź¹BaCl2×Ŗ»ÆĪŖĢ¼Ėį±µ³Įµķ£¬¹żĀĖŗó³Įµķ¼ÓČėŹŌ¼ĮbŃĪĖįæɽ«Ģ¼Ėį±µ×Ŗ»Æ³ÉBaCl2ČÜŅŗ£¬Č»ŗó¾Õō·¢”¢½į¾§”¢øÉŌļŗóæÉµĆ¹ĢĢåBaCl2£¬ČōŅŖ²ā¶ØŌ»ģŗĻĪļÖŠKClŗĶBaCl2µÄÖŹĮæ·ÖŹż£¬³żĮĖŅŖ×¼Č·³ĘĮæ»ģŗĻĪļµÄÖŹĮæĶā£¬ÖĮÉŁ»¹ŅŖ»ńµĆµÄŹż¾ŻŹĒ¹ĢĢåB»ņ³ĮµķA1µÄÖŹĮ棬ŅĄ¾ŻBĪŖBaCl2¼ĘĖćµĆµ½ÖŹĮæ·ÖŹż£¬A1ĪŖĢ¼Ėį±µ£¬½įŗĻ±µŌŖĖŲŹŲŗć¼ĘĖćĀČ»Æ±µÖŹĮæµĆµ½£¬
¹Ź“š°øĪŖ£ŗA1»ņB£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄ·ÖĄė”¢Ģį“æ²Ł×÷£¬ĪŖøßæ¼³£¼ūĢāŠĶ£¬²ąÖŲæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦ŗĶŹµŃéÄÜĮ¦£¬ĢāÄæÄŃ¶Č²»“ó£¬×¢Ņā°ŃĪÕĪļÖŹµÄŠŌÖŹ£¬øł¾ŻŠŌÖŹŃ”Ōń·“Ó¦ŹŌ¼Į£¬°ŃĪÕ»Æѧ»ł±¾ŹµŃé²Ł×÷ÖŖŹ¶£®


 ×Ö“Ź¾ä¶ĪĘŖĻµĮŠ“š°ø
×Ö“Ź¾ä¶ĪĘŖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃ鱹ŗÅ | 1 | 2 | 3 |
| ŹµŃé²½Öč | Č”Ņ»Š”ʬĀĖÖ½ÓƵķ·Ūµā»Æ¼ŲČÜŅŗŹŖČóŗ󣬷ÅŌŚ±ķĆęĆóÉĻ£¬ÖĆÓŚæÕĘųÖŠ£¬¹Ū²ģĻÖĻó | Č”Ņ»Š”ʬĀĖÖ½ÓƵķ·Ūµā»Æ¼ŲČÜŅŗŹŖČóŗ󣬷ÅŌŚ±ķĆęĆóÉĻ£¬ÖĆÓŚŃõĘųÖŠ£¬¹Ū²ģĻÖĻó | ȔɣĮæµķ·Ūµā»Æ¼ŲČÜŅŗÖĆÓŚŹŌ¹ÜÖŠ£¬ĶØĶł×ćĮæµÄĀČĘų£¬¹Ū²ģĻÖĻó |
| ŹµŃéĻÖĻó | ŹŌÖ½»ŗĀż±äĄ¶ | ŹŌÖ½²»±äĄ¶ | ČÜŅŗĻȱ䥶ŗóĶŹÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2£ŗ4£ŗ7 | B£® | 4£ŗ2£ŗ7 | C£® | 7£ŗ4£ŗ2 | D£® | 3£ŗ5£ŗ8 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
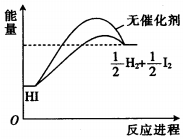
| A£® | ¼ÓČė“߻ƼĮ£¬¼õŠ”ĮĖ·“Ó¦µÄ»ī»ÆÄÜ | |
| B£® | ¼ÓČė“߻ƼĮ£¬æÉĢįøßHIµÄĘ½ŗā×Ŗ»ÆĀŹ | |
| C£® | ½µµĶĪĀ¶Č£¬HIµÄ·Ö½āĖŁĀŹ¼Óæģ | |
| D£® | ·“Ó¦ĪļµÄ×ÜÄÜĮæ“óÓŚÉś³ÉĪļµÄ×ÜÄÜĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
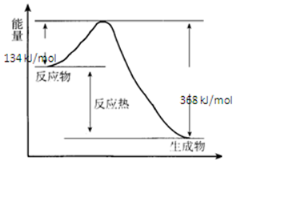 £Ø1£©ĻĀĮŠ·“Ó¦ÖŠ£¬ŹōÓŚĪüČČ·“Ó¦µÄŹĒ¢Ü¢Ż¢ß£®
£Ø1£©ĻĀĮŠ·“Ó¦ÖŠ£¬ŹōÓŚĪüČČ·“Ó¦µÄŹĒ¢Ü¢Ż¢ß£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
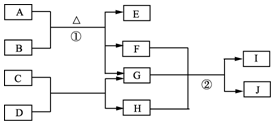 ÓŠ¹ŲĪļÖŹµÄ×Ŗ»Æ¹ŲĻµČēĶ¼1ĖłŹ¾£®AŹĒŗŚÉ«·Ē½šŹōµ„ÖŹ£¬C”¢E”¢F¾łĪŖŃõ»ÆĪļ£¬E”¢F³£ĪĀĻĀ³ŹĘųĢ¬£¬ĒŅEÄÜŹ¹Ę·ŗģĶŹÉ«£¬GŹĒŅ»ÖÖ³£¼ūµÄĪŽÉ«ŅŗĢ壬IŹĒŅ»ÖÖÄŃČÜÓŚĖ®µÄ°×É«½ŗד³Įµķ£¬ÄÜČÜÓŚBČÜŅŗ£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ÓŠ¹ŲĪļÖŹµÄ×Ŗ»Æ¹ŲĻµČēĶ¼1ĖłŹ¾£®AŹĒŗŚÉ«·Ē½šŹōµ„ÖŹ£¬C”¢E”¢F¾łĪŖŃõ»ÆĪļ£¬E”¢F³£ĪĀĻĀ³ŹĘųĢ¬£¬ĒŅEÄÜŹ¹Ę·ŗģĶŹÉ«£¬GŹĒŅ»ÖÖ³£¼ūµÄĪŽÉ«ŅŗĢ壬IŹĒŅ»ÖÖÄŃČÜÓŚĖ®µÄ°×É«½ŗד³Įµķ£¬ÄÜČÜÓŚBČÜŅŗ£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com