
医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙(含有少量Na+、Al3+、Fe3+等杂质)生产医药级二水合氯化钙(CaCl2·2H2O的质量分数为97.0%-103.0%)的主要流程如下:
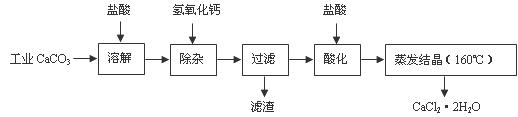
(1)除杂操作是加入氢氧化钙,调节溶液的pH为8.0-8.5,以除去溶液中的少量Al3+、Fe3+。检验Fe(OH)3是否沉淀完全的试验操作是 。
(2)酸化操作是加入盐酸,调节溶液的pH约为4.0,其目的有:①
;② 。
(3)测定样品中Cl- 含量的方法是:a.称取0.7500 g样品,溶解,在250 mL容量瓶中定容;b.量取25.00 mL待测溶液于锥形瓶中;c.用0.05000 mol·L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39 mL。
①计算上述样品中CaCl2·2H2O的质量分数为 。
②若用上述办法测定的样品中CaCl2·2H2O的质量分数有时超过100.0%(测定过程中产生的误差可忽略),其可能原因有
【知识点】物质分离和提纯的方法和基本操作综合应用;中和滴定.
【答案解析】(1)取少量上层清液与试管中(1分),滴加KSCN溶液,,若不出现血红色,则表明Fe(OH)3 沉淀完全(1分)。
(2)①将溶液中的少量Ca(OH)2转化为CaCl2;②防止溶液吸收空气中CO2
或者答:防止Ca2+在蒸发时水解(答到任意两个都给分)
(3)①99.91% (未保留四位有效数字扣一分) ②样品中存在少量的NaCl;少量的CaCl2·2H2O失水。
解析:(1)Fe3+与KSCN反应生成红色物质Fe(SCN)3,检验Fe3+是否存在应选用KSCN溶液,所需操作为取少量上层清液,滴加KSCN溶液,若不出现血红色,则表明Fe(OH)3 沉淀完全;
(2)因在除杂过程中加入了Ca(OH)2,故加入盐酸与溶液中的少量Ca(OH)2反应使其转化为CaCl2;另Ca(OH)2易吸收空气中的CO2,生成CaCO3沉淀,故加入盐酸还可以防止溶液吸收空气中CO2;
(3)
②样品中n(Cl-)=0.05000mol•L-1×0.02039L×10=0.010195mol,根据n(AgCl)=2n(CaCl2.2H2O),则
n(CaCl2.2H2O)=0.0050975mol,所以m(CaCl2.2H2O)=0.0050975mol×147g/mol=0.7493325g,
则有:0.7493325/0.7500×100%=99.9%;
③样品中存在少量的NaCl会导致CaCl2.2H2O的物质的量增大,同样若CaCl2.2H2O失水导致分母变小,值偏大。
【思路点拨】此题主要考查实验的基本操作、实验仪器的选择、实验误差分析.注意离子的检验方法和常见仪器的使用,样品纯度的分析要注意溶液中可能发生的反应,注意有效数字问题.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
对于反应:CaCO3+2HCl===CaCl2+H2O+CO2↑,下列说法正确的是( )
A.用HCl和CaCl2表示的反应速率数据不同,但所表示的意义相同
B.不能用CaCO3的浓度变化来表示反应速率,但可用水来表示
C.用H2O和CO2表示的化学反应速率相同
D.可以用CaCl2浓度的减小表示其反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
有Na2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的物质的量浓度为0.4 mol/L,SO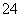 的物质的量浓度为0.7 mol/L,则此溶液中Na+的物质的量浓度为 ( )
的物质的量浓度为0.7 mol/L,则此溶液中Na+的物质的量浓度为 ( )
A.0.1 mol/L B.0.15 mol/L
C.0.2 mol/L D.0.25 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
配制250 mL 0.10 mol/L的NaOH溶液时,下列实验操作会使配得的溶液浓度偏大的是( )
 A.转移溶液后未洗涤烧杯和玻璃棒就直接定容
A.转移溶液后未洗涤烧杯和玻璃棒就直接定容
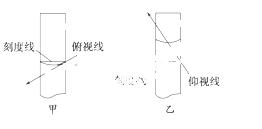
B.在容量瓶中进行定容时仰视刻度线
C.在容量瓶中定容时俯视刻度线
D.定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度
查看答案和解析>>
科目:高中化学 来源: 题型:
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若它们的温度和密度均相同,试根据甲、乙的摩尔质量(M)关系,判断下列说法正确的是
A.若M(甲)<M(乙),则气体的压强:甲>乙
B.若M(甲)>M(乙),则气体的摩尔体积:甲<乙
C.若M(甲)>M(乙),则气体体积:甲<乙
D.若M(甲)<M(乙),则分子数:甲<乙
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于氧化物的叙述不正确的是
①非金属氧化物不一定属于酸性氧化物 
②酸性氧化物都属于非金属氧化物
③金属氧化物都属于碱性氧化物 
④碱性氧化物都属于金属氧化物
⑤酸性氧化物都能与水反应生成相应的含氧酸
⑥两性氧化物既能与酸也能与碱反应生成盐和水
⑦与水反应生成含氧酸的氧化 物一定是酸性氧化物
物一定是酸性氧化物
⑧不能与酸反应的氧化物一定能与碱反应
A.①②③⑥⑧ B.②③⑤⑦⑧ C.②③⑤⑥⑦ D.②③④⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
现有下列物质:①Na2CO3 ②铜 ③氯化氢 ④CO2 ⑤NaHSO4 ⑥Ba(OH)2 ⑦氢氧化铁胶体 ⑧氨水 ⑨稀硝酸 ⑩KI
 (1)按物质的分类方法填写表格的空白处(填物质编号)
(1)按物质的分类方法填写表格的空白处(填物质编号)
| 分类标准 | 电解质 | 盐 | 非电解质 | 混合物 |
| 属于该类 的物质 |
(2)上述某两种物质在溶液中可发生离子反应:H++OH-= H2O,写出其中一个该离子反应对应的化学方程式 。
(3)物质⑩的稀溶液在空气中被氧化,加入淀粉溶液显蓝色,则反应的离子方程式为:

 ,
,
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下在一容积不变的密闭容器中发生可逆反应2X(g)  Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是 ( )
Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是 ( )
A.混合气体的密度不再变化
B.反应容器中Y的质量分数不变
C.X的分解速率与Y的消耗速率相等
D.单位时间内生成1 mol Y的同时生成2 mol X
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com