
分析 盐溶液中有弱才水解,明矾是硫酸铝钾,水溶液中溶解后,铝离子是弱碱阳离子,水溶液中水解溶液显酸性,小苏打是碳酸氢钠,溶液中碳酸氢根离子是弱酸阴离子,水溶液中水解显碱性,明矾和碳酸氢钠溶液混合,二者水解相互促进反应进行彻底生成氢氧化铝沉淀和二氧化碳气体;
解答 解:明矾是硫酸铝钾,水溶液中溶解后,铝离子是弱碱阳离子,水溶液中水解溶液显酸性,Al3++3H2O?Al(OH)3+3H+,小苏打是碳酸氢钠,溶液中碳酸氢根离子是弱酸阴离子,水溶液中水解显碱性,水解离子方程式为:HCO3-+H2O?H2CO3+OH-,明矾和碳酸氢钠溶液混合,二者水解相互促进反应进行彻底生成氢氧化铝沉淀和二氧化碳气体,反应现象为:有白色沉淀产生和无色气体放出,反应的离子方程式为:Al3++3HCO3-=Al(OH)3↓+3CO2↑,
故答案为:酸;Al3++3H2O?Al(OH)3+3H+;碱;HCO3-+H2O?H2CO3+OH-;有白色沉淀产生和无色气体放出;Al3++3HCO3-=Al(OH)3↓+3CO2↑.
点评 本题考查了盐类水解的原理,离子方程式书写,水解相互促进的反应进行彻底生成沉淀和气体,离子方程式书写用等号,需要标注沉淀和气体,题目较简单.


科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
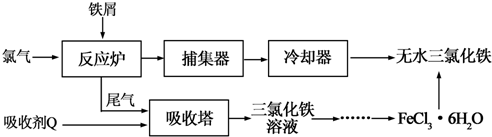
| 温度/℃ | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
| 溶解度(g/100gH2O) | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | pH=7 | B. | pH≥7 | C. | pH≤7 | D. | C(H+)•C(OH-)=10-14 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
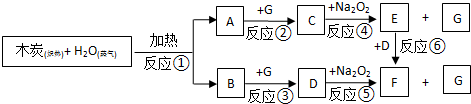
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 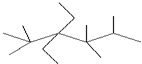 的系统命名为2,2,4,4,5-五甲基-3-二乙基己烷 的系统命名为2,2,4,4,5-五甲基-3-二乙基己烷 | |
| B. | 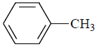 能使KMnO4溶液褪色,说明苯环与甲基相连的碳碳单键变得活泼,被KMnO4氧化而断裂 能使KMnO4溶液褪色,说明苯环与甲基相连的碳碳单键变得活泼,被KMnO4氧化而断裂 | |
| C. | 等物质的量的乙烯和乙醇的耗氧量相同 | |
| D. | 石油的分馏和煤的干馏都是物理变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com