
【题目】废水中氨态氮以NH3H2O、NH3和NH4+的形式存在,废水脱氮已成为主要污染物减排和水体富营养化防治的研究热点。
Ⅰ.沉淀法
向废水中投入MgCl2和Na2HPO4,生成MgNH4PO46H2O沉淀,可将氨态氮含量降至10mg·L1以下。
(1)NH3的电子式:______。
(2)废水中的NH3H2O转化为MgNH4PO46H2O的离子方程式是______。

(3)16℃时,向废水中加入MgCl2和Na2HPO4,使镁、氮、磷物质的量之比为1︰1︰1,沉淀过程中的pH对剩余氨态氮浓度的影响如图。欲使剩余氨态氮浓度低于10mg·L1,pH的适宜范围是______,pH偏大或者偏小均不利于MgNH4PO46H2O的生成,原因是______。
Ⅱ.微波—氧化法
(4)仅对废水进行微波加热,pH对氨态氮脱出的影响如下表。
溶液pH | 6~7 | 8~9 | 10~11 | 11~12 |
剩余氨态氮浓度(mg·L1) | 156 | 100 | 40 | 14 |
表中数据表明:pH增大有利于废水中化学平衡______(用化学用语表示)的移动。
(5)微波协同CuO和H2O2除去氨态氮
①其他条件相同,取相同体积的同一废水样品,微波10min,剩余氨态氮浓度与一定浓度H2O2溶液添加量的关系如下图。据图推测CuO在氨态氮脱除中可能起催化作用,理由是______。

②微波协同CuO有利于H2O2除去氨态氮。该条件下,H2O2将NH3氧化为N2的化学方程式是______。
【答案】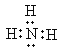 Mg2+ + NH3H2O+HPO42 + 5H2O = MgNH4PO46H2O↓ pH=8~10 pH偏大, NH4+、Mg2+易与OH结合生成NH3H2O、Mg(OH)2, NH3H2O的电离被抑制,使NH4+和Mg2+浓度降低;pH偏小,不利于HPO42电离,PO43浓度偏低。所以pH偏大或偏小均不利于MgNH4PO46H2O的生成 NH3+ H2O
Mg2+ + NH3H2O+HPO42 + 5H2O = MgNH4PO46H2O↓ pH=8~10 pH偏大, NH4+、Mg2+易与OH结合生成NH3H2O、Mg(OH)2, NH3H2O的电离被抑制,使NH4+和Mg2+浓度降低;pH偏小,不利于HPO42电离,PO43浓度偏低。所以pH偏大或偏小均不利于MgNH4PO46H2O的生成 NH3+ H2O![]() NH3H2O
NH3H2O![]() NH4+ + OH 相同的H2O2溶液添加量,相同时间内,与不加CuO相比,加入CuO,氨态氮浓度降低的多,反应速率快 3H2O2+ 2NH3
NH4+ + OH 相同的H2O2溶液添加量,相同时间内,与不加CuO相比,加入CuO,氨态氮浓度降低的多,反应速率快 3H2O2+ 2NH3![]() N2+6H2O
N2+6H2O
【解析】
(1)N原子最外层有5个电子,据此书写NH3的电子式;
(2)根据题意,废水中的NH3H2O转化为MgNH4PO46H2O,据此书写反应的离子方程式;
(3)由图可以判断欲使剩余氨态氮浓度低于10mg·L1的pH适宜范围;根据pH对NH4+、Mg2+、PO43浓度的影响分析解答;
(4)根据废水中存在NH3H2O,结合氨水的性质分析解答;
(5)①根据图像对比添加了CuO和未添加CuO的反应速率,以及氨态氮浓度的高低分析解答;
②在微波协同CuO作用下,H2O2和NH3生成N2,据此书写反应的方程式。
(1)NH3的电子式为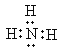 ,故答案为:
,故答案为: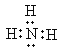 ;
;
(2)根据题意,废水中的NH3H2O转化为MgNH4PO46H2O,反应的离子方程式为Mg2+ + NH3H2O+HPO42 + 5H2O = MgNH4PO46H2O↓,故答案为:Mg2+ + NH3H2O+HPO42 + 5H2O = MgNH4PO46H2O↓;
(3)由图可以看出,欲使剩余氨态氮浓度低于10mg·L1,pH适宜范围为8~10,pH偏大, NH4+、Mg2+易与OH结合生成NH3H2O、Mg(OH)2, NH3H2O的电离被抑制,使NH4+和Mg2+浓度降低;pH偏小,不利于HPO42电离,PO43浓度偏低。所以pH偏大或偏小均不利于MgNH4PO46H2O的生成,故答案为:pH=8~10;pH偏大, NH4+、Mg2+易与OH结合生成NH3H2O、Mg(OH)2, NH3H2O的电离被抑制,使NH4+和Mg2+浓度降低;pH偏小,不利于HPO42电离,PO43浓度偏低。所以pH偏大或偏小均不利于MgNH4PO46H2O的生成;
(4)由表格数据可知,仅对废水进行微波加热,剩余氨态氮浓度降低、水溶液的pH增大,pH的增大,有利于废水中NH3+ H2O![]() NH3H2O
NH3H2O![]() NH4+ + OH逆向移动,故答案为:NH3+ H2O
NH4+ + OH逆向移动,故答案为:NH3+ H2O![]() NH3H2O
NH3H2O![]() NH4+ + OH;
NH4+ + OH;
(5)①由图可知,在相同时间和H2O2溶液添加量相同时,添加了CuO的反应速率较快,氨态氮的剩余浓度远远小于未添加CuO,故答案为:相同的H2O2溶液添加量,相同时间内,与不加CuO相比,加入CuO,氨态氮浓度降低的多,反应速率快;
②根据上述分析,在微波协同CuO作用下,H2O2和NH3生成N2,反应的方程式为3H2O2+ 2NH3![]() N2+6H2O,故答案为:3H2O2+ 2NH3
N2+6H2O,故答案为:3H2O2+ 2NH3![]() N2+6H2O。
N2+6H2O。


科目:高中化学 来源: 题型:
【题目】向三份0.1 ![]()
![]() , 溶液中分别加入少量
, 溶液中分别加入少量![]() 、
、![]() 、
、![]() 固体(忽略溶液体积变化),则
固体(忽略溶液体积变化),则![]() 浓度的变化依次为( )。
浓度的变化依次为( )。
A. 减小、增大、减小 B. 增大、减小、减小
C. 减小、增大、增大 D. 增大、减小、增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的体积不变的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。
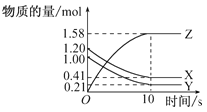
(1)写出该反应的化学方程式:________。
(2)从反应开始到10s,用Z表示的反应速率为________mol·L-1·s-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
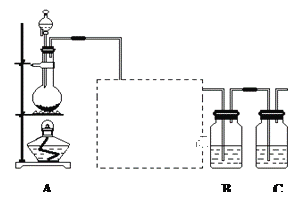
(1)装置A的分液漏斗中盛装的试剂是___________,烧瓶中加入的试剂是___________,发生的离子反应方程式_____________________;
(2)虚线框内是一个装有未知试剂的广口瓶,该试剂是___________,说明装置的作用________________;
(3)装置B中盛放的试剂是______________(选填下列所给试剂的字母),实验现象为___________________,化学反应方程式是__________________________________;
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4)已知:①硫酸比次氯酸稳定;②高氯酸比硫酸酸性强;③S2-比Cl-易被氧化;④HCl比H2S稳定;⑤铜与盐酸不反应,但能与浓硫酸反应;⑥铁与氯气加热生成三氯化铁,铁与硫加热生成硫化亚铁。可说明氯比硫非金属性强的是_________;
A.全部 B.②③④⑥ C.①②④⑤⑥ D.除①以外
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制![]() 溶液。回答下列问题:
溶液。回答下列问题:
(1)需要固体NaCl________g。
(2)配制操作中,一定用不到的玻璃仪器是________![]() 填选项字母
填选项字母![]() 。还缺少的玻璃仪器是________。
。还缺少的玻璃仪器是________。
A.烧杯 ![]() 胶头滴管
胶头滴管 ![]() 玻璃棒
玻璃棒 ![]() 分液漏斗
分液漏斗
(3)若容量瓶中有少量蒸馏水,所配溶液的浓度将________![]() 填“偏大”、“偏小”或“无影响”,下同
填“偏大”、“偏小”或“无影响”,下同![]() ;若定容时仰视加水至刻度线,所配溶液的浓度将________。
;若定容时仰视加水至刻度线,所配溶液的浓度将________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有反应PCl5(g)![]() PCl3(g)+Cl2(g),523K时,将10mol PCl5注入容积为2L的密闭容器中,平衡时压强为原来的1.5倍。
PCl3(g)+Cl2(g),523K时,将10mol PCl5注入容积为2L的密闭容器中,平衡时压强为原来的1.5倍。
(1)该温度下该反应的平衡常数K为________
(2)PCl5的平衡转化率为________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“封管实验”具有简易、方便、节约、绿色等优点,下列关于三个“封管实验”(夹持装置未画出)的说法正确的是( )
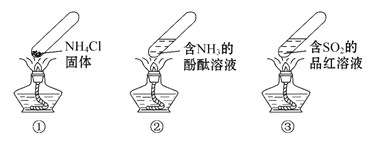
A. 加热时,①中上部汇集了NH4Cl固体
B. 加热时,②中溶液变红,冷却后又都变为无色
C. 加热时,③中溶液红色褪去,冷却后溶液变红,体现SO2的漂白性
D. 三个“封管实验”中所发生的化学反应都是可逆反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2SO2(g) + O2(g) ![]() 2SO3(g) △H =-akJ/mol(a>0),能量变化如图所示,下列说法不正确的是
2SO3(g) △H =-akJ/mol(a>0),能量变化如图所示,下列说法不正确的是

A. 2SO2(g) +O2(g) ![]() 2SO3(1) △H>-a kJ/mol
2SO3(1) △H>-a kJ/mol
B. 过程II可能使用了催化剂,使用催化剂不可以提高SO2的平衡转化率
C. 反应物断键吸收能量之和小于生成物成键释放能量之和
D. 将2molS02(g)和1 mol 02(g)置于一密闭容器中充分反应后放出的热量小于a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海藻中含有丰富的碘元素(以I-形式存在)。实验室中提取碘的流程如图:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ―→
―→![]()
(1)实验操作③的名称是__,所用主要仪器名称为__。
(2)提取碘的过程中,可供选择的有机试剂是___(填编号)。选择的理由是___。
A.酒精(沸点78℃) B.四氯化碳(沸点77℃)
C.甘油(沸点290℃) D.苯(沸点80℃)
(3)从碘的有机溶液中得到单质碘的方法是___。
(4)步骤①灼烧海藻时,除需要三脚架外,还需要用到的实验仪器是__(从下列仪器中选出所需的仪器,将字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com