
在100℃时,将0.100mol的N2O4气体充入1L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如下表格:
| 时间/s 浓度mol•L﹣1 | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)mol•L﹣1 | 0.100 | c1 | 0.050 | c3 | a | b |
| c(NO2)/mol•L﹣1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
试填空:
(1)达到平衡时N2O4的转化率为 %.
(2)20s的四氧化二氮的浓度c1= mol•L﹣1,在0s~20s内四氧化二氮的平均反应速率为 mol•(L•s)﹣1;.
考点:
化学平衡的计算.
专题:
化学平衡专题.
分析:
(1)由表可知,60s时反应达平衡,根据方程式计算△c(N2O4),根据转化率计算平衡时N2O4的转化率;60s后反应达平衡,反应混合物各组分的浓度不变;
(2)由△c(NO2),根据方程式计算△c(N2O4),20s的四氧化二氮的浓度=起始浓度﹣△c(N2O4);根据v= 计算v(N2O4).
计算v(N2O4).
解答:
解:(1)由表可知,60s时反应达平衡,c(NO2)=0.120mol/L,
N2O4⇌2 NO2,
浓度变化:0.06mol/L 0.120mol/L
所以平衡时N2O4的转化率为 ×100%=60%,
×100%=60%,
故答案为:60;
(2)由表可知,20s时,c(NO2 )=0.060mol/L,所以
N2O4⇌2 NO2,
浓度变化:0.03mol/L 0.060mol/L
所以20s的四氧化二氮的浓度c1=0.1mol/L﹣0.03mol/L=0.07mol/L;
在0s~20s内四氧化二氮的平均反应速率为v(N2O4) ═0.0015mol•(L•s)﹣1,
═0.0015mol•(L•s)﹣1,
故答案为:0.07;0.0015.
点评:
本题考查化学平衡的有关计算应用,主要是平衡转化率、反应速率概念的计算应用,难度中等,注意基础知识的积累掌握.


科目:高中化学 来源: 题型:
下列有关元素及其化合物性质的比较正确的是( )
|
| A. | 原子半径:F<O<Al | B. | 稳定性:H2O<PH3<NH3 |
|
| C. | 酸性:H2CO3<H2SO4<H3PO4 | D. | 碱性:LiOH<NaOH<Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
)下列溶液中微粒的物质的量浓度关系正确的是( )
|
| A. | Ca(ClO)2溶液中:c(Ca2+)>c(ClO﹣)>c(OH﹣)>c(H+) |
|
| B. | 等体积、等物质的量浓度的NaX和弱酸HX混合:c(Na+)=c(X﹣)>c(OH﹣)=c(H+) |
|
| C. | 常温下,将25mL0.2mol/L的盐酸与100mL0.1mol/L的氨水混合,所得溶液中:c(NH4+)>c(Cl﹣)>c(NH3•H2O)>c(OH﹣)>c(H+) |
|
| D. | 将0.1mol/L的Na2S溶液与0.1mol/L的NaHS溶液等体积混合,所得溶液中:c(S2﹣)+2c(OH﹣)=2c(H+)+c(HS﹣)+3c(H2S) |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应既属于氧化还原反应,又属于吸热反应的是( )
|
| A. | 铝片和稀盐酸反应 | B. | Ba(OH)2•8H2O与NH4Cl的反应 |
|
| C. | 甲烷在氧气中的燃烧反应 | D. | 灼热的碳与二氧化碳的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,往容积恒定的密闭容器中投入2molA和1molB,发生可逆反应:2A(g)+B(g)⇌C(g)+D(s),达到平衡时,测得压强为原压强的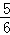 ,则A的转化率为( )
,则A的转化率为( )
|
| A. | 25% | B. | 40% | C. | 50% | D. | 75% |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是(NA表示阿伏伽德罗常数)( )
①36g D2O含有的质子数为18NA
②16g O2和O3混合物中含氧原子数为NA
③6.4g Cu与过量浓硫酸反应,可得到2.24L SO2
④在标准状况下,22.4L CO2和SO2混合气体中含有原子数为3NA
⑤10L PH=12的NaClO溶液含Na+0.1NA
⑥在标准状况下,22.4L Cl2溶解于足量的水中,转移电子数为NA.
A. ①②⑥ B. ①③⑤ C. ①②④ D. ③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中错误的是( )
A. 质量相等,密度不等的N2和C2H4两种气体含有的分子数一定相等
B. 同温同压下,等体积的H2和He气含有的质子数相等
C. 某物质经分析仅含一种元素,此物质可能是纯净物也可能是混合物
D. FeCl3溶液呈电中性,Fe(OH)3胶体带有电荷
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应原理不符合工业冶炼金属实际情况的是( )
A. 2HgO 2Hg+O2↑ B. 2NaCl(熔融)
2Hg+O2↑ B. 2NaCl(熔融) 2Na+Cl2↑
2Na+Cl2↑
C. 2MgO(熔融)  2Mg+O2↑ D. Fe2O3+3CO
2Mg+O2↑ D. Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com