
下列实验装置或操作设计正确、且能达到目的的是
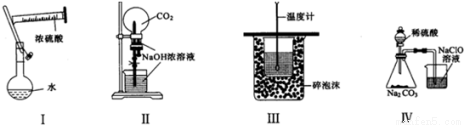
A.实验Ⅰ:配制一定物质的量浓度的稀硫酸
B.实验Ⅱ:用二氧化碳作喷泉实验
C.实验Ⅲ:进行中和热的测定
D.实验Ⅳ:验证酸性的强弱,H2SO4>H2CO3>HClO
科目:高中化学 来源:2015-2016学年湖南省高二下期中理科化学试卷(解析版) 题型:选择题
下列离子方程式正确的是()
A.铝溶于NaOH溶液:Al+2OH-= A1O2-+H2↑
B.铜溶于稀硝酸:3Cu+8H++2NO3-= 3Cu2++2NO↑+4H2O
C.碳酸镁中滴加稀盐酸:CO32-+2H+= CO2↑+H2O
D.稀硫酸中滴加氢氧化钡溶液:H++OH-= H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏银川二中高二下期中化学试卷(解析版) 题型:选择题
有机物甲的分子式为C9H18O2,在酸性条件下甲水解为乙和丙两种有机物,在相同的温度和压强下,同质量的乙和丙的蒸气所占体积相同,则甲的可能结构有( )
A.10种 B.14种 C.16种 D.18种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏银川二中高二下期中化学试卷(解析版) 题型:选择题
有机物大多易挥发,因此许多有机物保存时为避免挥发损失,可加一层水即“水封”,下列有机物可以用“水封法”保存的是( )
A.乙醇 B.氯仿 C.乙醛 D.乙酸乙酯
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三5月模拟考试理综化学试卷(解析版) 题型:实验题
K2SO4是无氯优质钾肥,Mn3O4是生产磁性氧体材料的主要原料,以硫酸工业的尾气联合制备K2SO4和Mn3O4的工艺流程如下:

(1)几种盐的溶解度见图2.反应Ⅲ中,向(NH4)2SO4溶液中加入KCl溶液充分反应后,进行蒸发浓缩、________、洗涤、干燥等操作即得K2SO4产品。
(2)检验K2SO4样品是否含有氯化物杂质的实验操作是______________________________;
(3)反应Ⅳ的化学方程式为_____________________________;
(4)Mn3O4与浓盐酸加热时发生反应的离子方程式为_____________________________;
(5)图3煅烧MnSO4•H2O时温度与剩余固体质量变化曲线。
①该曲线中B段所表示物质的化学式为_______________________;
②煅烧过程中固体锰含量随温度的升高而增大,但当温度超过1000℃时,再冷却后,测得产物的总锰含量反而减小.试分析产物总锰含量减小的原因_______________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西吉安一中高二下第二次段考化学试卷(解析版) 题型:推断题
药物菲那西汀的一种合成路线如下:
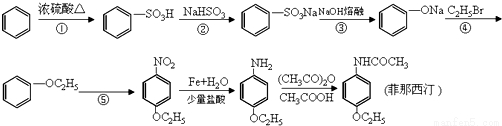
(1)菲那西汀的分子式_______________;
(2)反应②中生成的无机物的化学式为_______________;
(3)写出⑤反应的化学方程式_______________;
(4)菲那西汀水解的化学方程式是_______________;
(5)菲那西汀的同分异构体中,符合下列条件的共有_______种。
①含苯环且只有对位两个取代基 ②苯环上含有氨基 ③能水解,水解产物能发生银镜反应.
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西吉安一中高二下第二次段考化学试卷(解析版) 题型:选择题
已知:25℃时,Mg(OH)2的Ksp=5.61×10-12,MgF2的Ksp=7.42×10-11,下列判断正确的是
A.25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大
B.25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大
C.25℃时,Mg(OH)2固体在20 mL 0.01 mol•L-1氨水中的K比在20 mL 0.01 mol•L-1NH4Cl溶液中的K小
D.25℃时,在Mg(OH)2悬浊液中加入NaF溶液后,Mg(OH)2不可能转化为MgF2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高二下期中化学试卷(解析版) 题型:填空题
)卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。
(1)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的.使氢氟酸分子缔合的作用力是____________。
(2)请根据如表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是_________。
氟 | 氯 | 溴 | 碘 | 铍 | |
第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 | 900 |
(3)已知高碘酸有两种形式,化学式分别为H5IO6(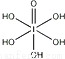 )和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6______HIO4(填“>”、“<”或“=”)。
)和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6______HIO4(填“>”、“<”或“=”)。
(4)碘在水中的溶解度虽然小,但在碘化钾溶液中溶解度却明显增大这是由于溶液中发生下列反应:I-+I2═I3-.I3-的中心原子周围的σ键电子对对数为______ 。与KI3类似的,还有CsICl2等。已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列________式发生。
A.CsICl2=CsCl+ICl B.CsICl2=CsI+Cl2
(5)已知CaF2晶体的密度为ρg·cm3,NA为阿伏加德罗常数,CaF2晶胞的边长为apm,则CaF2的相对分子质量可以表示为________________(用含a的式子表示)。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省黄冈市高三4月考试理综化学试卷(解析版) 题型:选择题
分析下列实验操作,其中可能不能达到实验目的的是( )
序号 | 实验操作 | 实验目的 |
① | 将足量的SO2气体通入装有品红溶液的试管中 | 研究SO2具有漂白性 |
② | 向盛有1mL AgNO3溶液的试管中滴加几滴NaCl溶液,再向其中滴加几滴Na2S溶液 | 比较Ksp(AgCl)与Ksp(Ag2S)的大小 |
③ | 测定等物质的量浓度的HCl、HNO3的pH | 比较Cl、N的非金属性强弱 |
④ | 向2支试管中加入同体积同浓度H2C2O4溶液,再分别加入同体积不同浓度的酸性KMnO4溶液 | 研究浓度对反应速率的影响 |
A.②③④ B.①③④ C.①②③④ D.①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com