
【题目】已知短周期元素的离子![]() 、
、![]() 、
、![]() 、
、![]() 都具有相同的电子层结构,则下列叙述正的是
都具有相同的电子层结构,则下列叙述正的是
A.原子半径A>B>D>CB.原子序数d>c>b>a
C.离子半径C>D>B>AD.单质的还原性A>B>D>C
【答案】C
【解析】
已知短周期元素的离子![]() 、
、![]() 、
、![]() 、
、![]() 都具有相同的电子层结构,则离子核外电子数相同,即a-2=b-1=c+3=d-1,原子序数A>B>D>C,A、B处于同一周期,C、D处于同一周期,且A、B处于C、D所在周期的相邻下一周期,A、B形成阳离子,则A、B为金属,C、D形成阴离子,则C、D为非金属。
都具有相同的电子层结构,则离子核外电子数相同,即a-2=b-1=c+3=d-1,原子序数A>B>D>C,A、B处于同一周期,C、D处于同一周期,且A、B处于C、D所在周期的相邻下一周期,A、B形成阳离子,则A、B为金属,C、D形成阴离子,则C、D为非金属。
A.A、B处于同一周期,C、D处于同一周期,且A、B处于C、D所在周期的相邻下一周期,同周期,原子序数越大原子半径越小,所以原子半径B>A,C>D,电子层越大原子半径越大,所以原子半径B>A>C>D,A错误;
B.![]() 、
、![]() 、
、![]() 、
、![]() 都具有相同的电子层结构,则离子核外电子数相同,即a-2=b-1=c+3=d-1,原子序数a>b>d>c,B错误;
都具有相同的电子层结构,则离子核外电子数相同,即a-2=b-1=c+3=d-1,原子序数a>b>d>c,B错误;
C.电子层结构相同,核电荷数越大,离子半径越小,核电荷数A>B>D>C,所以离子半径:C3->D->B+>A2+,C正确;
D.A、B处于同一周期,A、B形成阳离子,则A、B为金属,原子序数A>B,单质还原性B>A,C、D处于同一周期,C、D形成阴离子,则C、D为非金属,原子序数D>C,单质氧化性D>C,D错误。
答案选C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某种化合物(如图)由 W、X、Y、Z 四种短周期元素组成,其中 W、Y、Z 分别位于三个不同周期,Y 核外最外层电子数是 W 核外最外层电子数的二倍;W、X、Y 三种简单离子的核外电子排布相同。下列说法不正确的是
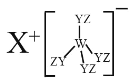
A.原子半径:W < X < Y < Z
B.X 与 Y、Y 与 Z 均可形成具有漂白性的化合物
C.简单离子的氧化性: W X
D.W 与 X 的最高价氧化物的水化物可相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(气)+B(气)![]() 2C(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2C(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示的反应平均速率为0.3 mol·L-1·s-1
②用物质B表示的反应的平均速率为0.6 mol·L-1·s-1
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7 mol·L-1
其中正确的是:
A.①③B.①④C.②③D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烷燃烧可以通过以下两种途径:
途径I:C3H8(g) + 5O2(g) == 3CO2(g) +4H2O(l) ΔH=-a kJ·mol-1
途径II:C3H8(g) ==C3H6(g)+ H2(g) ΔH=+b kJ·mol-1
2C3H6(g)+ 9O2(g) == 6CO2(g) +6H2O(l) ΔH=-c kJ·mol-1
2H2(g)+O2(g) == 2H2O(l) ΔH=-d kJ·mol-1(a、b、c、d均为正值)
请回答下列问题:
(1)判断等量的丙烷通过两种途径放出的热量,途径I放出的热量 ______(填“大于”、“等于”或“小于”)途径II放出的热量。
(2)由于C3H8(g) ==C3H6(g)+ H2(g) 的反应中,反应物具有的总能量______(填“大于”、“等于”或“小于”)生成物具有的总能量,那么在化学反应时。反应物就需要______(填“放出”、或“吸收”)能量才能转化为生成物,因此其反应条件是______________。
(3)b 与a、c、d的数学关系式是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水CuCl2为棕黄色固体,用于颜料、木材防腐等工业,并用作消毒剂、媒染剂、催化剂等。实验室用如图所示装置制取CuCl2。(夹持装置省略)
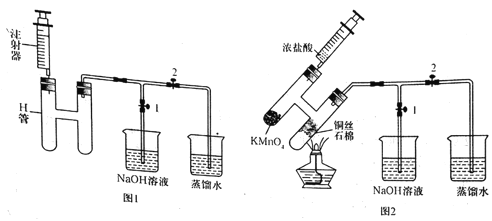
步骤1:制备时,首先按照图1所示连接实验装置。打开两处的止水夹,检验装置的气密性。
步骤2:用镊子向H管一端装入少量石棉,将其置于H管连通管以下部分且靠近连通管约![]() 处,将卷成团状的细铜丝置于石棉上。H管的另外一端装入少量KMnO4固体。在注射器中装入少量浓盐酸,待用。
处,将卷成团状的细铜丝置于石棉上。H管的另外一端装入少量KMnO4固体。在注射器中装入少量浓盐酸,待用。
步骤3:关闭止水夹2,打开止水夹1,将H管如图2所示倾斜放置,点燃酒精灯,加热铜丝直至其呈红热状态。立即将浓盐酸注入H管使其与KMnO4发生反应(注意调整H管倾斜度以利于浓盐酸的加入),观察到有黄绿色气体通过连通管部分进入H管另一端,继而与热铜丝燃烧得到产物。
待反应结束后,等待一段时间再打开止水夹2,关闭止水夹1,拉动注射器将蒸馏水慢慢的吸入H管中,在H管底部得到CuCl2溶液。最后进行尾气的处理操作。请回答以下有关问题。
(1)检验图1所示装置气密性时的操作方法是______。反应过程中将H管倾斜放置的目的是_________(写出一条即可)。
(2)浓盐酸与KMnO4反应的化学方程式为______。热铜丝燃烧得到产物时,铜丝上方的H管中观察到的现象是_____。反应结束后,“等待一段时间”再进行后续操作的原因是______。
(3)实验观察到蒸馏水慢慢地吸入H管中时,H管底部得到CuCl2溶液的颜色,有一个从黄绿色到绿色再到蓝绿色的变化过程。已知在溶液中[Cu(H2O)4]2+呈蓝色,[CuCl4]2-呈黄色。请用方程式表示溶液颜色变化的化学平衡体系:___。
(4)H管中铜丝不直接放置在右管底部的优点是___(写出两条即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在铝表面除去氧化膜,物理方法可用_________,化学方法可将其浸入氢氧化钠溶液,发生反应的化学方程式为:_________;
(2)将除去氧化膜的铝迅速用蒸馏水清洗干净,立即插入硝酸汞溶液片刻,发生反应的离子方程式为:__________________;取出铝片用滤纸吸去表面溶液,铝片上出现的“黑斑”是_________;
(3)将此铝放置于空气中,“黑斑”边会长出“白毛”,此物质是_________.
(4)此实验证明了(________)
A.氧化铝都是十分坚硬的晶体 B.铝是较活泼的金属,可以被空气中氧气氧化
C.铝表面的氧化膜有保护作用 D.铝是很不活泼的金属,不可以被氧气氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】双极膜由阳离子交换膜、催化剂层和阴离子交换膜组合而成,在直流电场作用下可将水解离,在双极膜的两侧分别得到H+和OH-,将其与阳离子交换膜(阳膜)、阴离子交换膜(阴膜)组合,可有多种应用。
(1)海水淡化:模拟海水淡化,双极膜组合电解装置示意图如下。

①X极是______极(填“阴”或“阳”)。
②电解后可获得较浓的盐酸和较浓的NaOH溶液,上图中双极膜的右侧得到的是______(填“H+”或“OH-”)。
(2)钠碱循环法脱除烟气中的SO2,并回收SO2:
用pH>8的Na2SO3溶液作吸收液,脱除烟气中的SO2,至pH<6时,吸收液的主要成分为NaHSO3,需再生。
Ⅰ.加热pH<6时的吸收液使其分解,回收SO2并再生吸收液。所得的再生吸收液对SO2的吸收率降低,结合离子方程式解释原因:______。
Ⅱ.双极膜和阴膜组合电渗析法处理pH<6时的吸收液,可直接获得再生吸收液和含较高浓度HSO3的溶液,装置示意图如下。

①再生吸收液从______室流出(填“A”或“B”)。
②简述含较高浓度HSO3的溶液的生成原理:______。
③与Ⅰ中的方法相比,Ⅱ中的优点是______(列出2条)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)相同物质的量浓度的①CH3COOH 溶液,②盐酸,c(H+)较大的是____________(填编号);CH3COOH 的电离方程式为____________。
(2)FeCl3溶液保存时需加少量____________(填“盐酸”或“硫酸”)。
(3)甲醇 CH3OH 是一种重要的化工原料,在生产中有着广泛的应用。合成 CH3OH 的一种 反应为:CO(g) + 2H2(g)![]() CH3OH (g)。一定条件下,将 1 mol CO 和 2 mol H2在 1L 容器中发生上述反应,经过 2 min 反应生成了 a mol CH3OH(反应前后体积不变)。
CH3OH (g)。一定条件下,将 1 mol CO 和 2 mol H2在 1L 容器中发生上述反应,经过 2 min 反应生成了 a mol CH3OH(反应前后体积不变)。
①此时 CO 的浓度为____________mol/L 。
②2min 内用 H2 表示该反应的速率为 v(H2) =____________mol/(L·min)。
③升高温度,反应的平衡常数 K 减小,则该反应为____________(填“吸热反应”或“放热反应”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 、
、![]() 、
、![]() 、
、![]() 为前20号元素且原子序数依次增大,元素
为前20号元素且原子序数依次增大,元素![]() 和
和![]() 同族。盐
同族。盐![]() 与浓盐酸反应,有黄绿色气体产生,
与浓盐酸反应,有黄绿色气体产生,![]() 的焰色反应为浅紫色。下列说法正确的是( )
的焰色反应为浅紫色。下列说法正确的是( )
A.原子半径大小为![]()
B.![]() 简单氢化物的沸点低于
简单氢化物的沸点低于![]() 简单氢化物的沸点
简单氢化物的沸点
C.![]() 与
与![]() 均含有非极性键
均含有非极性键
D.标准状况下,单质![]() 与单质
与单质![]() 的状态相同
的状态相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com