
 �������ڹ���Ԫ��Fe��Ti����C��H��N��O�γɶ��ֻ����
�������ڹ���Ԫ��Fe��Ti����C��H��N��O�γɶ��ֻ�������� ��1���ٸ���Ԫ�����ڱ��縺�Եĵݱ���ɱȽϵ縺��ǿ����
�ڷ����к����ǻ�����ˮ�����γ������������̼Ϊsp�ӻ�������̼̼������6���Ҽ��������6��̼��Ҽ���
��̼Ϊ�ļۣ���Ϊ���ۣ���Ϊ���ۣ����ᣨHOCN����һ����״���ӣ���������ڸ�ԭ���������Ѵﵽ�ȶ��ṹ����N��C-O-H��
��2�����γ������Ӿ߱�������Ϊ������ԭ�Ӿ��пչ����������й¶Ե��Ӷԣ�
���������������[Fe��CN��6]4-��Fe2+��CN-�γ���λ����CN-�д���C��N��������������1���Ҽ�2���м���CN-��Cԭ����1����λ�������Nԭ���滻�ɵ�CN-�ȵ�����ĵ��ʣ�
��3������Tiԭ�Ӻ�������Ų�ʽ���
��4���ٸ��ݾ�̯�����㻯ѧʽ��
�ڼ���������߳������ɽ�һ��������������Feԭ��֮��ľ��룮
��� �⣺��1����ͬ����Ԫ�ش�����Ԫ�صĵ縺�����������е縺��C��N��O��H�ĵ縺����С���縺��˳��Ϊ��H��C��N��O���ʴ�Ϊ��H��C��N��O��
��a����ȩ�к����ǻ�����ˮ�����γ��������a��ȷ��
b��HCHO������Cԭ�Ӳ���sp2�ӻ�����������̼������Cԭ��Ϊsp�ӻ�����b����
c��C2H2��ֱ���ͶԳƽṹ��Ϊ�Ǽ��Է��ӣ�������̼̼������6���Ҽ���ÿ��̼�������һ���Ҽ�����������һ������12������c����
d��������̼�����Ƿ��Ӿ��壬�������辧����ԭ�Ӿ��壬����CO2������۵㡢�е㶼�ȶ������辧��ĵͣ���d��ȷ��
�ʴ�Ϊ��bc��
�����ᣨHOCN����һ����״���ӣ���������ڸ�ԭ���������Ѵﵽ�ȶ��ṹ��̼Ϊ�ļۣ���Ϊ���ۣ���Ϊ���ۣ���N��C-O-H���ʴ�Ϊ��N��C-O-H��
��2�����γ������Ӿ߱�������Ϊ������ԭ�Ӿ��пչ����������й¶Ե��Ӷԣ��ʴ�Ϊ�����й¶Ե��ӣ�
���������������[Fe��CN��6]4-��Fe2+��CN-�γ���λ����CN-�д���C��N������Ϊ���Թ��ۼ�����������1���Ҽ�2���м�������CN-�й��ۼ�����λ�����Ҽ����м���CN-��Cԭ����1����λ�������Nԭ���滻�ɵ�CN-�ȵ�����ĵ���ΪN2���ʴ�Ϊ��B��N2��
��3��Tiԭ�Ӻ�������Ų�Ϊ1s22s22p63s23p63d24s2����λ�ڵ������ڵڢ�B�壬����d�����ʴ�Ϊ��d��
��4����Feλ�ڶ��㡢���ġ����ĺ����ģ���ĿΪ8��$\frac{1}{8}$+6��$\frac{1}{2}$+1+12��$\frac{1}{4}$=8��Alλ�ھ������ģ���ĿΪ4��ԭ����Ŀ��ֵΪ2��1����ѧʽ��дΪ��Fe2Al��
�ʴ�Ϊ��Fe2Al��
�ھ�������Ϊ��$\frac{4}{{N}_{A}}$����56��2+27��g���辧���߳�Ϊa cm�������Ϊa3cm3�����ܶȹ�ʽ�ã��ѡ�a3=$\frac{4}{{N}_{A}}$����56��2+27�������a=2$\root{3}{\frac{139}{2��{N}_{A}}}$������Feԭ��֮��ľ���Ϊ�߳���һ�룬�����Ϊ��$\frac{1}{2}$��a cm=$\root{3}{\frac{139}{2��{N}_{A}}}$cm���ʴ�Ϊ��$\root{3}{\frac{139}{2��{N}_{A}}}$��
���� ���⿼�������ʽṹ�����ʣ���Ŀ�Ƚ��ۺϣ����ض����ʽṹ����֪ʶ�Ŀ��飬�漰�縺�ԡ��ӻ����ۡ���ѧ�������ӽṹ�����ʡ��������������ʡ���������ȣ���Ҫѧ���߱���ʵ�Ļ���֪ʶ���Ѷ��еȣ�


 ��ѧ����ͬ����ϰϵ�д�
��ѧ����ͬ����ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
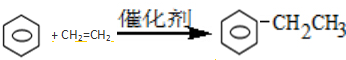 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
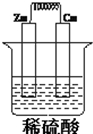 ��ͼ��ʾ����п��ͭͨ����������������ϡ�����й���ԭ��أ�����¿�
��ͼ��ʾ����п��ͭͨ����������������ϡ�����й���ԭ��أ�����¿��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ֻ�Т٢� | B�� | �����ⶼ�� | C�� | ֻ�Т٢� | D�� | ֻ�Т٢ܢޢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֪�����ۻ���Ϊ6.0 kJ/mol�������������Ϊ20 kJ/mol������1 mol������2 mol ��������ۻ�����ȫ�����ƻ���������������ֻ���ƻ�����15%����� | |
| B�� | ����CaCO3��s���TCaO��s��+CO2��g�� �κ��¶��¶������Է����� | |
| C�� | ʵ���û����飨l��������ϩ��l���ͱ���l���ı�ȼ���ȷֱ�Ϊ-3916 kJ/mol��-3747 kJ/mol��-3265 kJ/mol������֤���ڱ������в����ڶ�����̼̼˫�� | |
| D�� | ��֪��Fe2O3��s��+3C��ʯī���T2Fe��s��+3CO��g������H=+489.0 kJ/mol�� CO��g��+$\frac{1}{2}$O2��g���TCO2��g������H=-283.0 kJ/mol�� C��ʯī��+O2��g���TCO2��g������H=-393.5 kJ/mol�� ��4Fe��s��+3O2��g���T2Fe2O3��s������H=-1641.0 kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1H��D��T����ͬһ�ֺ��� | |
| B�� | ���й��ۼ��Ļ�����һ���ǹ��ۻ����� | |
| C�� | NH4Cl�ĵ���ʽΪ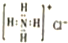 | |
| D�� | S2-�Ľṹʾ��ͼΪ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ����/�� | ��A | ��A | ��A | ��A | ��A | ��A | ����A | 0 |
| 2 | �� | �� | �� | �� | ||||
| 3 | �� | �� | �� | �� | �� |
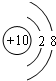 ��
��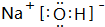 �������ʽ�����������еĻ�ѧ�����������Ӽ������Թ��ۼ�����ѡ�����Ӽ����������Թ��ۼ��������Ǽ��Թ��ۼ����е�һ������д����
�������ʽ�����������еĻ�ѧ�����������Ӽ������Թ��ۼ�����ѡ�����Ӽ����������Թ��ۼ��������Ǽ��Թ��ۼ����е�һ������д����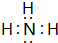 ����ˮ��Һ�ʼ��ԣ�����ԡ��������ԡ����ԡ�����
����ˮ��Һ�ʼ��ԣ�����ԡ��������ԡ����ԡ������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ƺ�̼�����Ʒ�Ӧ������ṹ��ͬʱ����-OH��-COOH | |
| B�� | ���������к�������-CH3������������̼���� | |
| C�� | ���������нṹ�в���ֻ����C-O����C-H�� | |
| D�� | ��1mol C3H6O3�������Ʒ�Ӧֻ����1mol������˵��һ����C3H6O3�к���2��-OH��һ��-CHO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���Ṥҵ����Ӧ�����ۺϾ���Ч�����⣮
���Ṥҵ����Ӧ�����ۺϾ���Ч�����⣮| 1������ѹ | 5������ѹ | 10������ѹ | 15������ѹ | |
| 400�� | 0.9961 | 0.9972 | 0.9984 | 0.9988 |
| 500�� | 0.9675 | 0.9767 | 0.9852 | 0.9894 |
| 600�� | 0.8520 | 0.8897 | 0.9276 | 0.9468 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com