
【题目】【化学一选修5:有机化学基础】
某高聚物W和树脂X的合成路线如下:
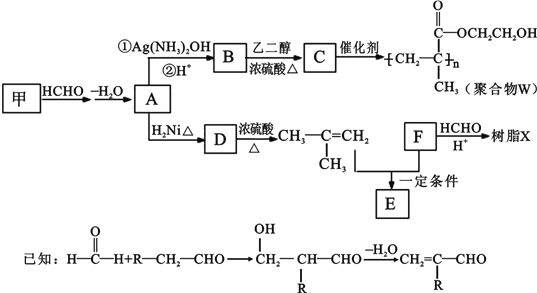
(1) A 的结构简式是_____。
(2) C中含氧官能团的名称是_____。
(3) D 的名称是_____。
(4) A→B 的第一步化学反应方程式是__
(5) 已知 F 的相对分子质量为 110,分子中碳原子、氢原子数都是氧原子数的 3 倍,苯环上的氢原子化学环境都相同,则 F 能发生的反应是(填字母)___。
a.加成反应 b.加聚反应 c.氧化反应 d.水解反应
(6) E 的分子式为 C10H14O2,含三个甲基,苯环上的一溴代物有两种。生成 E 的化学方程式是_____。
(7) B 有多种同分异构体。属于酯且含有碳碳双键的同分异构体共有__种(不考虑顺反异构)。
【答案】 ![]() 酯基,羟基 2-甲基-1-丙醇
酯基,羟基 2-甲基-1-丙醇 ![]() + 2Ag(NH3)2OH
+ 2Ag(NH3)2OH ![]()
![]() COONH4 + H20 +2Ag↓ +3NH3 ac
COONH4 + H20 +2Ag↓ +3NH3 ac 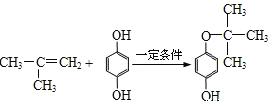 5
5
【解析】由合成路线可知,利用逆推法结合W可知,C为CH2=C(CH3)COOCH2CH2OH,B与乙二醇发生酯化反应生成C,则B为CH2=C(CH3)COOH,A→B发生氧化反应,则A为CH2=C(CH3)CHO,A→D发生加成反应,D为CH3CH(CH3)CH2OH,结合已知信息可知,甲为醛,与HCHO反应再脱水生成A,则甲为CH3CH2CHO,F的相对分子质量为110,分子中碳原子、氢原子数都是氧原子数的3倍,苯环上的氢原子化学环境都相同,则F为![]() ,E的分子式为C10H14O2,含三个甲基,苯环上的一溴代物有两种,则2-甲基丙烯与F发生加成反应生成E,E为
,E的分子式为C10H14O2,含三个甲基,苯环上的一溴代物有两种,则2-甲基丙烯与F发生加成反应生成E,E为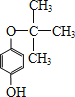 。
。
(1)由上分析知A为CH2=C(CH3)CHO;(2)C为CH2=C(CH3)COOCH2CH2OH,C中含氧官能团是酯基和羟基;(3)D为CH3CH(CH3)CH2OH,名称为:2-甲基-1-丙醇;(4)A→B发生氧化反应,CH2=C(CH3)CHO + 2Ag(NH3)2OH ![]() CH2=C(CH3)COONH4 + H2O +2Ag↓ +3NH3;(5)F为
CH2=C(CH3)COONH4 + H2O +2Ag↓ +3NH3;(5)F为![]() ,能发生加成反应和氧化反应;(6)B为CH2=C(CH3)COOH,属于酯且含有碳碳双键的同分异构体有HCOOCH=CHCH3、HCOOC(CH3)=CH2、CH3COOCH=CH2、CH2=CHCOOCH3、HCOOCH2CH=CH2,共5种。
,能发生加成反应和氧化反应;(6)B为CH2=C(CH3)COOH,属于酯且含有碳碳双键的同分异构体有HCOOCH=CHCH3、HCOOC(CH3)=CH2、CH3COOCH=CH2、CH2=CHCOOCH3、HCOOCH2CH=CH2,共5种。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】用两支惰性电极插入500mLAgNO3溶液中,通电电解。当电解液的c(H+)从1×10-6molL-1变为1×10-3molL-1时(设电解时阴极没有氢气析出且电解液在电解前后体积变化可以忽略不计),电极上析出银的质量约是()
A. 27mg B. 54mg C. 108mg D. 216mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO: MgSO4(s)+CO(g) ![]() MgO(s)+CO2(g)+SO2(g) △H >0,该反应在某密闭容器中达到平衡。下列分析正确的是
MgO(s)+CO2(g)+SO2(g) △H >0,该反应在某密闭容器中达到平衡。下列分析正确的是
A. 恒温恒容时,充入CO气体,达到新平衡时![]() 增大
增大
B. 容积不变时,升高温度,混合气体的平均相对分子质量减小
C. 恒温恒容时,分离出部分SO2气体可提高MgSO4的转化率
D. 恒温时,增大压强平衡逆向移动,平衡常数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H、N、O、Na、S、Cl都是中学化学中的常见元素,根据题意回答与这些元素有关的问题:
(1)画出Na原子结构示意图_______,Na2O2可用作供氧剂,其电子式为_______。
(2)Cl2是一种大气污染物,装有液氯的钢瓶上应贴的标签是_______(填编号)。
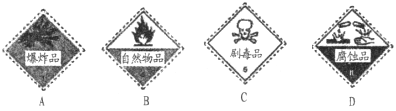
氯气泄漏可用NaHSO3溶液来处理,写出相关的离子反应方程式_____________。
(3)25C时,利用pH试纸测得0.1mol/L氨水的pH约为11,则可以估算出氨水的电离常数约为_____;向10mL此溶液中通入少量氨气,忽略溶解过程中溶液温度和体积的微小变化,溶液中![]() 将_______(填“增大” “减小”或“无法确定”)。
将_______(填“增大” “减小”或“无法确定”)。
(4)有两种化合物同时含有上述六元素中的四种元素。将这两种化合物的溶液混合后,恰好完全反应,生成物之一M仍含有这四种元素,该反应的离子方程式为______________。若M溶液的pH =5,则由水电离出的c(H+)=_______mol/L,该溶液离子浓度由大到小的顺序为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证氧化性Cl2>Fe3+> SO2,某小组用下图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验)。
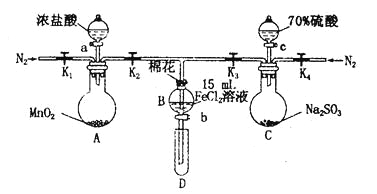
实验过程:
I.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,关闭K2。
Ⅳ.打开活塞b,使约2 mL的溶液流入D试管中,检验其中的离子。
V.打开K3和活塞c,加入70%的硫酸,一段时间后关闭K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程I的目的是____。
(2)检验B中溶液是否还有Fe2+的方法之一是:取少量B中溶液于试管中,滴加几滴含有+3价铁元素的配合物溶液,会产生蓝色沉淀.写出该反应的离子方程式____ 。
(3)若向第III步B中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的离子方程式____。
(4)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的化学方程式为________。
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定不能够证明氧化性Cl2>Fe3+>SO2的是____(填“甲”、“乙”或“丙”)。
过程Ⅳ,B溶液中含有的离子 | 过程Ⅵ,B溶液中 含有的离子 | |
甲 | 有Fe3+无Fe2+ | 有SO42- |
乙 | 既有Fe3+又有Fe2+ | 有SO42- |
丙 | 有Fe3+无Fe2+ | 有Fe2+ |
(6)将B中的FeCl2溶液换成100 mLFeBr2溶液并向其中通入1.12 LCl2(标准状况下),若溶液中有1/2的Br一被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为____ mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】植物油厂想要提取大豆中丰富的油脂,下列方案设计合理的是( )
A.将大豆用水浸泡,使其中的油脂溶于水,然后再分馏
B.先将大豆压成颗粒状,再用无毒的有机溶剂浸泡,然后对浸出液进行蒸馏分离
C.将大豆用碱溶液处理,使其中的油脂溶解,然后再蒸发出来
D.将大豆粉碎,然后隔绝空气加热,使其中的油脂挥发出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将少量金属钠投入到氯化铁溶液中,产物是
A. Fe(OH)3、NaCl,H2
B. Fe,NaCl
C. NaOH、H2
D. H2、NaCl、NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com