
| A. | 原子半径:R>Q | B. | R和Q可形成离子化合物R2Q5 | ||
| C. | R和Q可形成共价化合物RQ | D. | R和Q可形成共价化合物RQ2 |
分析 R、Q为短周期中的两种元素,R元素原子的最外层电子数与次外层电子数之差的绝对值等于电子层数,若电子层数为2,最外层电子数为4,R为C元素,若电子层数为3,最外层电子数为5,R为P元素;Q元素原子的最外层电子数是次外层电子数的3倍,若Q为第二周期元素,Q为O元素,且Q不可能为第三周期元素,以此来解答.
解答 解:由上述分析可知,R为C或P,Q为O,
A.若R为P,Q为O,电子层越多,原子半径越大,则原子半径:R>Q,故A正确;
B.R和Q可形成共价化合物P2O5,不含离子键,故B错误;
C.若R为C,R和Q可形成共价化合物CO,故C正确;
D.R和Q可形成共价化合物CO2,故D正确;
故选B.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构、电子排布规律来推断元素为解答的关键,侧重分析与推断能力的考查,注意规律性知识的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 直径介于1nm~100nm之间的微粒称为胶体 | |
| B. | 电泳现象可证明胶体带电 | |
| C. | 渗析法可用于含有氯化钠的淀粉溶液的提纯 | |
| D. | 用含1molFeCl3的溶液可制得6.02×1023个Fe(OH)3胶体粒子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X 与 Y 形成化合物时,X 可能显负价,也可能显正价 | |
| B. | 第一电离能 X 可能小于 Y | |
| C. | X 的最高价含氧酸的酸性强于 Y 的最高价含氧酸的酸性 | |
| D. | 原子序数 X 一定大于 Y |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
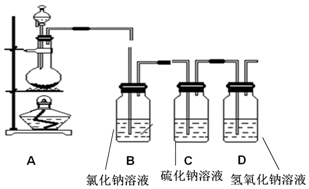
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+、Na+、SO42-、Cl- | B. | K+、Na+、Cl-、NO3- | ||
| C. | Mg2+、Ca2+、CO32-、NO3- | D. | OH-、Fe3+、Ca2+、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液中:Na+、Fe2+、NO3-、SO42- | |
| B. | 水电离出的c(H+)=1×10-12mol•L-1的溶液中:K+、Al3+、Cl-、SO42- | |
| C. | 加入酚酞溶液显红色的溶液中:Na+、K+、HCO3-、Cl- | |
| D. | 无色溶液中:K+、NH4+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将0.4mol/LNH4Cl溶液和0.2molNaOH溶液等体积混合后,溶液中粒子的物质的量浓度大小关系为:c(NH4+)>c(Na+)>c(NH3•H2O)>c(OH-)>c(H+) | |
| B. | SiO2(s)+2C(s)═Si(s)+2CO(g)在常温下不能自发进行,则该反应的△H>0 | |
| C. | 物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合后的溶液中:2c(Na+)═c(CH3COO-)+c(CH3COOH) | |
| D. | 在相同条件下,NaHCO3溶液和NaHSO3溶液中,水的电离平衡均被促进 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A. | 反应在前50s的平均速率为v(PCl3)=0.001 6 mol•L-1•s-1 | |
| B. | 保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11 mol•L-1,则反应的△H>0 | |
| C. | 相同温度下,起始时向容器中充入1.0 molPCl5、0.20 molPCl3和0.20 molCl2,达到平衡前v(正)>v(逆) | |
| D. | 相同温度下,起始时向容器中充入2.0 molPCl3、2.0 molCl2,达到平衡时,PCl3的转化率大于80% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石墨转变成碳纳米管为物理变化 | |
| B. | “滴水石穿,绳锯木断”不包含化学变化 | |
| C. | 232Th转化为233U是化学变化 | |
| D. | 将地沟油制成肥皂是化学变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com