
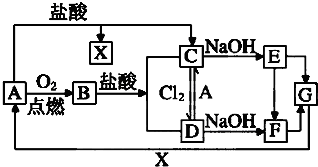
 已知A是一种常见金属,F是一种红褐色沉淀.试根据图中转化关系,回答下列问题.
已知A是一种常见金属,F是一种红褐色沉淀.试根据图中转化关系,回答下列问题.

科目:高中化学 来源: 题型:
| A、FeBr3溶液中加入过量的氯水 2Fe2++4Br-+3Cl2=2Br2+6Cl-+2Fe3+ |
| B、向小苏打溶液中加入醋酸 CO32-+2CH3COOH=CO2↑+H2O+2CH3COO- |
| C、向碳酸钠溶液中加入少量氯水 CO32-+2H+=CO32-+H2O |
| D、用碳酸钠溶液吸收少量二氧化硫 2CO32-+SO2+H2O=2HCO3-+SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
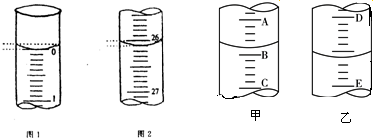 下面a~e是中学化学实验中常见的几种定量仪器:
下面a~e是中学化学实验中常见的几种定量仪器:查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 没有现象发生 |
| ② | B+D | 有气体放出 |
| ③ | B+C | 有沉淀生成 |
| ④ | A+D | 有沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ⑤CH≡CH
⑤CH≡CH查看答案和解析>>
科目:高中化学 来源: 题型:
| A、V(H2)═0.1mol/(L?min) |
| B、V(N2)═0.1mol/(L?min) |
| C、V(NH3)═0.15mol/(L?min) |
| D、V(N2)═0.002mol/(L?s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2B溶液一定有:c(OH-)>c(H+)+c(HB-) |
| B、Na2B溶液一定呈碱性,NaHB溶液可能呈酸性也可能呈碱性 |
| C、NaHB溶液一定有:c(Na+)+c(H+)=c(HB-)+c(OH-)+c(B2-) |
| D、NaHB溶液一定呈酸性,Na2B溶液一定呈碱性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com