
| A£® | 100ml 0.1mol/LµÄĀČĖ®ÖŠĶØČė0.01molSO2ĘųĢå | |
| B£® | 100ml 0.5mol/LµÄNaOHÖŠĶØČė0.005molĀČĘų | |
| C£® | 100ml 0.5mol/LµÄCuSO4ČÜŅŗÖŠ¼ÓČė4g NaOH¹ĢĢå | |
| D£® | 100ml×ŌĄ“Ė®ÖŠ¼ÓČė0.01molÕįĢĒČܽā |
·ÖĪö ČÜŅŗµÄµ¼µēŠŌÓėĄė×ÓÅØ¶Č³ÉÕż±Č£¬ÓėµēŗɳÉÕż±Č£¬ÄÜŹ¹ČÜŅŗµ¼µēŠŌ±ä»Æ½Ļ“ó£¬ĖµĆ÷²Ł×÷Ē°ŗóČÜŅŗÖŠĄė×ÓÅØ¶Č±ä»Æ½Ļ“󣬾Ż“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗA£®ĀČĖ®ÖŠHClOŹĒĒæµē½āÖŹ”¢HClŹĒĒæµē½āÖŹ£¬ĒŅĀČĘųµÄČܽāŠŌ½ĻŠ”£¬ĖłŅŌ0.1mol/LµÄĀČĖ®ÖŠČÜŅŗµÄµ¼µēŠŌ½ĻČõ£¬ĶØČė0.01mol¶žŃõ»ÆĮņŗó£¬ĀČĘų”¢Ė®ŗĶ¶žŃõ»ÆĮņ·¢ÉśŃõ»Æ»¹Ō·“Ӧɜ³ÉŃĪĖįŗĶĮņĖį£¬Ąė×ÓÅØ¶Č±ä»Æ½Ļ“ó£¬ČÜŅŗµ¼µēŠŌ±ä»Æ½Ļ“󣬹ŹAÕżČ·£»
B£®NaOHŹĒĒæµē½āÖŹ£¬100ml 0.5mol/LµÄNaOHÖŠĶØČė0.005molĀČĘų£¬¶žÕß·“Ó¦ŗóČÜŅŗÖŠČÜÖŹĪŖNaCl”¢NaClO”¢NaOH£¬Ąė×ÓÅØ¶Č±ä»Æ²»“ó£¬ČÜŅŗµ¼µēŠŌ±ä»Æ²»“󣬹ŹB“ķĪó£»
C£®n£ØNaOH£©=$\frac{4g}{40g/mol}$=0.1mol£¬¶žÕßĶźČ«·“Ӧɜ³ÉĒāŃõ»ÆĶŗĶĮņĖįÄĘ£¬Ąė×ÓÅØ¶Č±ä»Æ²»“ó£¬ČÜŅŗµ¼µēŠŌ±ä»Æ²»“󣬹ŹC“ķĪó£»
D£®ÕįĢĒŹĒ·Ö×Ó¾§Ģ壬ČÜÓŚĖ®ŗóŅŌ·Ö×Ó“ęŌŚ£¬ĖłŅŌ×ŌĄ“Ė®ÖŠĄė×ÓÅØ¶Č±ä»Æ²»“ó£¬ŌņČÜŅŗµ¼µēŠŌ±ä»Æ²»“󣬹ŹD“ķĪó£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éµē½āÖŹČÜŅŗµ¼µēŠŌĒæČõÅŠ¶Ļ£¬ĪŖøßĘµæ¼µć£¬Ć÷Č·Ąė×ÓÅØ¶Č”¢Ąė×ÓĖł“ųµēŗÉŹĒÓ°ĻģČÜŅŗµ¼µēŠŌÖ÷ŅŖŌŅņŹĒ½ā±¾Ģā¹Ų¼ü£¬ÖŖµĄĪļÖŹÖ®¼ä·¢ÉśµÄ·“Ó¦¼°ĒæČõµē½āÖŹ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 mol/L CaCl2ČÜŅŗÖŠŗ¬ÓŠCl-µÄŹżÄæĪŖNA | |
| B£® | ±ź×¼×“æöĻĀ£¬2.24L HFĖłŗ¬·Ö×ÓŹżŅ»¶ØĪŖ0.1NA | |
| C£® | 6.4g S6ÓėS8µÄ»ģŗĻĪļÖŠĖłŗ¬SŌ×ÓŹżŅ»¶ØĪŖ0.2NA | |
| D£® | ±ź×¼×“æöĻĀ£¬2.24L ŃõŌŖĖŲµÄµ„ÖŹĖłŗ¬Ō×ÓŹżŅ»¶ØĪŖ0.2NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃ鱹ŗÅ | ĪĀ¶Č | 0 | 10 | 20 | 40 | 50 | |
| 1 | 130”ę | n£ØCH4£©/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| 2 | 180”ę | n£ØCH4£©/mol | 0.50 | 0.30 | 0.18 | 0.15 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaNO2 | B£® | AgNO3 | C£® | BaCO3 | D£® | BaSO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 |  |  |  |
| A | B | C | D |
| A | B | C |
 |  |  |
| NH3 | CO2 | CCl4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ż | B£® | ¢Ś¢Ū¢Ž | C£® | ¢Ś¢Ż¢Ž | D£® | ¢Ł¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
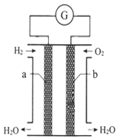 ĒāŃõČ¼ĮĻµē³ŲŹĒŅ»ÖÖ»ÆѧµēŌ“£¬ČēĶ¼ĖłŹ¾£¬ŅŌŹÆÄ«ĪŖµē¼«£¬Į½¼«·Ö±šĶØČėĒāĘųŗĶŃõĘų£¬KOHČÜŅŗĪŖµē½āÖŹČÜŅŗ£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
ĒāŃõČ¼ĮĻµē³ŲŹĒŅ»ÖÖ»ÆѧµēŌ“£¬ČēĶ¼ĖłŹ¾£¬ŅŌŹÆÄ«ĪŖµē¼«£¬Į½¼«·Ö±šĶØČėĒāĘųŗĶŃõĘų£¬KOHČÜŅŗĪŖµē½āÖŹČÜŅŗ£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | ŌŚµē³Ų·“Ó¦ÖŠĆæ×ŖŅĘ2molµē×Ó£¬Õż¼«ĻūŗÄO2µÄĢå»żĪŖ11.2L | |
| B£® | b¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗO2+2H2O+4e-ØT4OH- | |
| C£® | ¹¤×÷Ņ»¶ĪŹ±¼äŗ󣬵ē½āÖŹČÜŅŗ¼īŠŌ¼õČõ | |
| D£® | øĆ×°ÖĆ½«»ÆѧÄÜ×Ŗ»ÆĪŖµēÄÜ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com