
【题目】【2016盐城三模】实验室制取高纯NaI晶体(无色)可按下列步骤进行:按化学计量称取各原料,在三颈烧瓶中(如图)先加入适量的高纯水,然后按Na2CO3、I2和水合肼的投料顺序分批加入.
已知:①I2+Na2CO3═NaI+NaIO+CO2↑;△H<0
3I2+3Na2CO3═5NaI+NaIO3+3CO2↑;△H<0
②I2(s)+I﹣(aq)═I3﹣(aq);
③水合肼(N2H4H2O)具有强还原性,可分别将IO﹣、IO3﹣和I2还原为I﹣,本身被氧化为N2(放热反应);100℃左右水合肼分解为氮气和氨气等.
(1)常温常压时,I2与Na2CO3溶液反应很慢,下列措施能够加快反应速率的是 (填字母).
a.将碘块研成粉末 b.起始时加少量NaI
c.将溶液适当加热 d.加大高纯水的用量
(2)I2与Na2CO3溶液反应适宜温度为40~70℃,温度不宜超过70℃,除防止反应速率过快,另一个原因是 .
(3)加入稍过量水合肼发生反应的离子方程式为 (只写一个).
(4)整个实验过程中都需要开动搅拌器,其目的是 .
(5)反应的后期I2与Na2CO3溶液反应难以进行,此阶段需对投料顺序作适当改进,改进的方法是 .
(6)所得溶液(偏黄,且含少量SO42﹣,极少量的K+和Cl﹣)进行脱色、提纯并结晶,可制得高纯NaI晶体.实验方案为:在溶液中加入少量活性炭煮沸、
(实验中需使用的试剂有:HI溶液,Na2CO3溶液、Ba(OH)2溶液、高纯水及pH试纸;除常用仪器外须使用的仪器有:真空干燥箱)。

【答案】(1)abc (2)防止碘升华 (3)2IO﹣+N2H4+H2O=2I﹣+N2+3H2O (4)使得合成反应均匀进行,并使产生的二氧化碳、氮气等气体及时排除 (5)先加入碘、水合肼,最后加入碳酸钠 (6)趁热过滤将滤液在不断搅拌下依次加入稍过量的氢氧化钡、碳酸钠溶液,过滤,滤液中在不断搅拌下加入HI溶液至使用pH试纸测定溶液的pH大约为6,蒸发冷却结晶,再次过滤,用高纯度的水洗涤晶体2﹣3次,在真空干燥箱中干燥
【解析】(1)a.将碘块研成粉末,增加接触面积,可以加快反应速率,故正确;b.起始时加少量NaI,可以起到催化剂的作用,加快反应速率,故正确;c.将溶液适当加热可以加快反应速率,故正确;d.加大高纯水的用量,降低浓度会降低反应速率,故错误,故选abc;
(2)I2与Na2CO3溶液反应适宜温度为40~70℃,温度不宜超过70℃,这样可以防止碘单质受热易升华;
(3)NaIO在水溶液中可以和肼发生氧化还原反应生成NaI、氮气和水,即2IO﹣+N2H4+H2O=2I﹣+N2+3H2O;
(4)结合搅拌器的搅拌作用,整个实验过程中都需要开动搅拌器,其目的是可以使混合物均匀混合,将产生的气体及时的排出;
(5)根据反应:I2+Na2CO3═NaI+NaIO+CO2↑;△H<0,3I2+3Na2CO3═5NaI+NaIO3+3CO2↑;△H<0,后期I2与Na2CO3溶液反应难以进行,碘单质的浓度减小导致的,此阶段可以先加入碘、水合肼,最后加入碳酸钠;
(6)所得溶液含少量SO42﹣,极少量的K+和Cl﹣,首先除杂,依次加入稍过量的氢氧化钡、碳酸钠溶液,过滤,然后,调整溶液的酸碱性,进行蒸发结晶操作,进行物质的分离和提纯,即趁热过滤将滤液在不断搅拌下依次加入稍过量的氢氧化钡、碳酸钠溶液,过滤,滤液中在不断搅拌下加入HI溶液至使用pH试纸测定溶液的pH大约为6,蒸发冷却结晶,再次过滤,用高纯度的水洗涤晶体2﹣3次,在真空干燥箱中干燥。


科目:高中化学 来源: 题型:
【题目】某化学实验小组选用图所示装置和下列所给试剂来证明非金属性:Cl>I. 
请你按照他们的设计思路完成该实验.
【可供选择的试剂有】
①稀盐酸,②浓硫酸,③MnO2 , ④浓盐酸,⑤淀粉碘化钾溶液,⑥KMnO4 , ⑦NaOH溶液,⑧硝酸银溶液.
烧瓶A中应盛放的药品是(填序号),试管C中应盛放的药品是(填序号),则装置D的作用是 , 当观察到现象 , 即可证明非金属性Cl>I.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法不正确的是( )
A.常温下,100g46%乙醇水溶液中含有H原子数为12 NA
B.23gNa与足量O2反应,生成Na2O 和Na2O2的混合物,转移的电子数为 NA
C.标准状况下,2.24 LCCl4含有的共价键数为0.4 NA
D.1 molN2与4molH2反应生成的NH3分子数小于2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的颜色状态描述正确的是 ( )
A. NO2—— 无色气体 B. BaSO4 ——灰绿色固体
C. Al(OH)3 —— 白色固体 D. H2O —— 白色液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】英国天文学家在人马座附近发现了一片酒精云,这片酒精云的质量达100万亿亿吨.现有如图转化关系,下列说法不正确的是( ) ![]()
A.N为乙酸
B.可用饱和碳酸钠溶液除去乙酸乙酯中混有的N
C.过程①中可加入LiAlH4等还原剂将乙醇转化为N
D.过程②如果加热一段时间后发现忘记加碎瓷片,应停止反应,待冷却后补加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于实验基本操作的叙述不正确的是( )
A. 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
B. 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
C. 将浓硫酸倒入盛水的量筒中稀释成稀硫酸
D. 使用容量瓶、分液漏斗前,先检查是否漏水后洗涤干净
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2017硚口区校级模拟】某兴趣小组为探究外界条件对可逆反应A(g)+B(g)═C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10L的密闭容器中充入1mol A和1mol B,反应达平衡时测得容器中各物质的浓度为Ⅰ.然后改变不同条件做了另三组实验,重新达到平衡时容器中各成分的浓度分别为Ⅱ、Ⅲ、Ⅳ.
A | B | C | |
Ⅰ | 0.050molL﹣1 | 0.050molL﹣1 | 0.050molL﹣1 |
Ⅱ | 0.070molL﹣1 | 0.070molL﹣1 | 0.098molL﹣1 |
Ⅲ | 0.060molL﹣1 | 0.060molL﹣1 | 0.040molL﹣1 |
Ⅳ | 0.080molL﹣1 | 0.080molL﹣1 | 0.12molL﹣1 |
针对上述系列实验,下列结论中错误的是( )
A.由Ⅰ中数据可计算出该温度下反应的平衡常数K=20mol﹣1L
B.Ⅱ可能是通过增大C的浓度实现的
C.若Ⅲ只是升高温度,则与Ⅰ比较,可以判断出正反应一定是放热反应
D.第Ⅳ组实验数据的得出,只能通过压缩容器的体积才可以实现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下0.1molC12溶于水,转移的电子数目为0.1NA
B. 1 L 0.1 molL-1氯化铁溶液中铁离子数为0.1NA
C. 0.1 molNa2O2与足量的潮湿的二氧化碳反应转移的电子数为0.1NA
D. 标准状况下,2.24LNO和2.24LO2混合后气体分子数一定为0.15NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2017孝义市模拟】在体积为2L的恒容密闭容器中发生反应xA(g)+yB(g)zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A)n(B)的变化关系.则下列结论正确的是( )
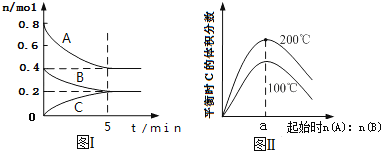
A.200℃时,反应从开始到平衡的平均速率v(B)=0.04molL﹣1min﹣1
B.图Ⅱ所知反应xA(g)+yB(g)zC(g)的△H<0,且a=2
C.若在图Ⅰ所示的平衡状态下,再向体系中充入He,重新达到平衡前v(正)>v(逆)
D.200℃时,向容器中充入2 mol A 和1 mol B,达到平衡时,A 的体积分数小于50%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com