
无水氯化铝是一种重要的化工原料,利用明矾石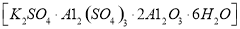 制备无水氯化铝的流程如下:
制备无水氯化铝的流程如下:
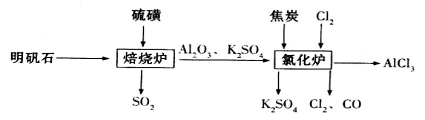
(1)验证焙烧炉产生的气体含有SO2的方法是________________________________。
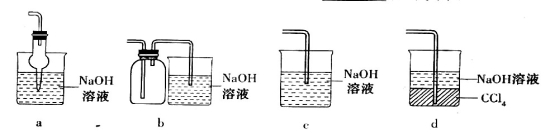
(2)吸收焙烧炉中产生的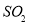 ,下列装置合理的是________(填代号)。
,下列装置合理的是________(填代号)。
(3)氯化炉中发生反应的化学方程式为_________________________________________。
(4)生产氯化铝的过程中产生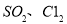 等大气污染物,若将二者按照一定比例通入水中可减少或消除污染。试设计简单实验检验二者是否恰好完全反应。(简要描述实验步骤、现象和结论)____________。
等大气污染物,若将二者按照一定比例通入水中可减少或消除污染。试设计简单实验检验二者是否恰好完全反应。(简要描述实验步骤、现象和结论)____________。
仪器自选;可供选择试剂如下:
①滴加酚酞的氢氧化钠溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④品红溶液
(5)某学习小组设计用如下装置验证二氧化硫的某些化学性质。

①能说明二氧化硫具有氧化性的实验现象为_____________________________________。
②写出a瓶中发生反应的离子方程式___________________________________________。
③充分反应后,取a瓶中的溶液分成三份,分别进行如下实验。
实验I:向第一份溶液中加入足量的NaOH溶液,生成白色沉淀,迅速变为灰绿色,最终变为红褐色
实验II:向第二份溶液中加入少量KMnO4溶液,紫色褪去
实验III:向第三份溶液中加入BaC12溶液,生成白色沉淀
上述实验中能证明二氧化硫具有还原性的是________(填实验代号)。
(1)将气体通入品红溶液中,若品红溶液褪色,加热后又变红,证明有SO2;(2)a、d;(3)3C+Al2O3+3Cl2 3CO+2AlCl3;(4)取所得溶液少许置于试管中,向其中加入品红溶液,若平衡溶液不褪色,说明二者恰好完全反应;否则,二者未完全反应;(5)①b中出现淡黄色浑浊(或B中生成淡黄色沉淀)②2Fe3++SO2+2H2O=SO42-+2Fe2++4H+;③I和II。
3CO+2AlCl3;(4)取所得溶液少许置于试管中,向其中加入品红溶液,若平衡溶液不褪色,说明二者恰好完全反应;否则,二者未完全反应;(5)①b中出现淡黄色浑浊(或B中生成淡黄色沉淀)②2Fe3++SO2+2H2O=SO42-+2Fe2++4H+;③I和II。
【解析】
试题分析:(1)验证焙烧炉产生的气体含有SO2的方法是利用SO2的漂白性,将气体通入品红溶液中,若品红溶液褪色,加热后又变红,证明有SO2;(2)a. SO2容易与NaOH发生反应使导气管内的压强减小而引起倒吸现象,所以用干燥管既可以使气体充分吸收,也防止了倒吸现象的发生,正确;b容易引起倒吸,使溶液进入到集气瓶内,错误;c.容易引起倒吸,使溶液进入到集气瓶内,错误;d. SO2不能在CCl4在溶解,从导气管内出来后既在水中溶解,也防止了倒吸现象的发生,正确。(3)根据框图中物质之间的转化关系可知:在氯化炉中发生反应的化学方程式为3C+Al2O3+3Cl2 3CO+2AlCl3;(4)生产氯化铝的过程中产生SO2 、Cl2等大气污染物,若将二者按照一定比例通入水中二者会发生反应:Cl2+SO2+2H2O=H2SO4+2HCl,因此可减少或消除污染。若二者恰好完全反应,则产物中只有硫酸和盐酸,若不完全反应,可能Cl2过量,也可能SO2过量,无论哪一种过量,溶液都具有漂白性,所以检验方法是取所得溶液少许置于试管中,向其中加入品红溶液,若平衡溶液不褪色,说明二者恰好完全反应;否则,二者未完全反应;(5)①能说明二氧化硫具有氧化性的实验现象为b中Na2S溶液中出现淡黄色浑浊;②在a瓶中Fe3+将SO2氧化为硫酸,发生反应的离子方程式是2Fe3++SO2+2H2O=SO42-+2Fe2++4H+;③实验I:向第一份溶液中加入足量的NaOH溶液,生成白色沉淀,迅速变为灰绿色,最终变为红褐色,证明溶液中存在Fe2+,说明SO2有还原性;实验II:向第二份溶液中加入少量KMnO4溶液,紫色褪去,说明SO2有还原性;实验III:向第三份溶液中加入BaC12溶液,生成白色沉淀BaSO4,与SO2有还原性还是氧化性无关,因此;上述实验中能证明二氧化硫具有还原性的是I和II。
3CO+2AlCl3;(4)生产氯化铝的过程中产生SO2 、Cl2等大气污染物,若将二者按照一定比例通入水中二者会发生反应:Cl2+SO2+2H2O=H2SO4+2HCl,因此可减少或消除污染。若二者恰好完全反应,则产物中只有硫酸和盐酸,若不完全反应,可能Cl2过量,也可能SO2过量,无论哪一种过量,溶液都具有漂白性,所以检验方法是取所得溶液少许置于试管中,向其中加入品红溶液,若平衡溶液不褪色,说明二者恰好完全反应;否则,二者未完全反应;(5)①能说明二氧化硫具有氧化性的实验现象为b中Na2S溶液中出现淡黄色浑浊;②在a瓶中Fe3+将SO2氧化为硫酸,发生反应的离子方程式是2Fe3++SO2+2H2O=SO42-+2Fe2++4H+;③实验I:向第一份溶液中加入足量的NaOH溶液,生成白色沉淀,迅速变为灰绿色,最终变为红褐色,证明溶液中存在Fe2+,说明SO2有还原性;实验II:向第二份溶液中加入少量KMnO4溶液,紫色褪去,说明SO2有还原性;实验III:向第三份溶液中加入BaC12溶液,生成白色沉淀BaSO4,与SO2有还原性还是氧化性无关,因此;上述实验中能证明二氧化硫具有还原性的是I和II。
考点:考查有关SO2的性质、检验、化学方程式和离子方程式的书写的知识。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2015届山东省德州市高三10月月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.酸式盐的水溶液一定显酸性
B.酸性氧化物一定是非金属氧化物
C.丁达尔效应是溶液和胶体的本质区别
D.HClO是弱酸,但NaClO是强电解质
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三11月阶段模块考试化学试卷(解析版) 题型:选择题
下列有关化学实验叙述正确的是
A.容量瓶、滴定管、分液漏斗使用前都必须检查是否漏水
B.用98%的浓硫酸配制100g10%的稀硫酸时,除使用量筒外还需用到容量瓶
C.在钠跟水反应的实验中,切下绿豆粒大小的钠投入水中进行实验,剩余的钠块丢弃到废料桶中
D.若FeCl2溶液中含有I-杂质,可用过量Cl2氧化后进行萃取分液
查看答案和解析>>
科目:高中化学 来源:2015届山东省乐陵市高三10月初检测化学试卷(解析版) 题型:选择题
某混合液中含有等物质的量的CuSO4、FeSO4、Fe2(SO4)3。已知下表数据:
物质(25℃) | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
完全沉淀时的pH | ≥6.4 | ≥9.6 | 3~4 |
下列叙述正确的是
A.混合溶液中:c(SO42-):[ c(Cu2+) +c(Fe3+) +c(Fe2+)]=5:4
B.若向混合溶液中加入铁粉,不可能观察到红色固体析出
C.若向混合溶液中加入足量氯水,调节pH到3~4后过滤,得到纯净的CuSO4溶液
D.若向混合溶液中逐滴加入烧碱溶液,首先生成Fe(OH)3沉淀
查看答案和解析>>
科目:高中化学 来源:2015届山东省乐陵市高三10月初检测化学试卷(解析版) 题型:选择题
用下列分离装置进行相应实验,能达到相应实验目的的是
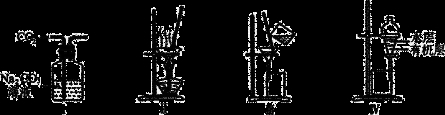
A.用图Ⅰ所示装置除去CO2中含有的少量HCl
B.用图Ⅱ所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C.用图Ⅲ所示装置分离NaCl和Na2SO4的混合溶液
D.用图Ⅳ所示装置分离CCl4萃取碘水中的碘后已分层的有机层和水层
查看答案和解析>>
科目:高中化学 来源:2015届山东省临沂市高三10月份月考化学试卷(解析版) 题型:选择题
下列过程最终无沉淀产生的是( )
A.过量氨气通入Al2(SO4)3溶液 B.CO2通入CaCl2溶液
C.少量SO2通入BaCl2溶液后再通入过量Cl2 D.过量CO2通入Na2SiO3溶液
查看答案和解析>>
科目:高中化学 来源:2015届山东省临沂市高三10月份月考化学试卷(解析版) 题型:选择题
C、N、S都是重要的非金属元素,下列说法正确的是
A.三者对应的氧化物均为酸性氧化物
B.实验室可用NaOH溶液处理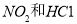 废气
废气
C.三者的单质直接与氧气反应都能生成两种氧化物
D.CO2、NO2、SO2都能与H2O反应,其反应原理相同
查看答案和解析>>
科目:高中化学 来源:2015届山东淄博市高三上学期第二次诊断性检测理综化学试卷(解析版) 题型:选择题
用下图所示装置进行下列实验,能达到实验目的的是

A.瓶中盛有适量浓H2SO4,从A口进气来干燥NH3
B.从B口进气,用排空气法收集CO2
C.瓶中盛满水,从B口进气,用排水法收集NO2
D.瓶中装满水,A口连接导管并伸入量筒中,从B口进气,用排水法测量生成H2的体积
查看答案和解析>>
科目:高中化学 来源:2015届安徽省高二上学期期中考试化学试卷(解析版) 题型:选择题
CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都属于离子型碳化物。请通过CaC2制C2H2的反应进行思考,从中得到必要的启示,判断下列反应产物正确的是
A.ZnC2水解生成乙烷 B.Al4C3水解生成丙炔
C.Mg2C3水解生成丙炔 D.Li2C2水解生成乙烯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com