
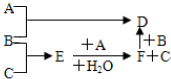
分析 有A、B、C三种常见单质,其有关反应如图所示:已知B、E的水溶液显酸性,E在一定条件下有还原性,但不能被浓H2SO4氧化,B显黄绿色为Cl2,D遇KSCN溶液显血红色,判断含有Fe3+,确定D为FeCl3,A为Fe,C为H2,E为HCl,F为FeCl2,据此分析回答.
解答 解:(1)C为H2,氢原子形成共价键,氢气的电子式为:H:H,
故答案为:H:H;
(2)A+B→D反应为铁和氯气反应生成氯化铁,反应的方程式为:2Fe+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3,
故答案为:2Fe+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3.
点评 本题考查了无机物的性质分析判断,转化关系的理解应用,主要是铁及其化合物性质的分析,掌握据此是解题关键,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | 46gNO2和N2O4的混气体中,含氮原子数目是NA | |
| B. | 1.0L 0.1mol/L的NaF溶液中,含F-离子数目是0.1NA | |
| C. | 11.2L的H2中,含有的电子数目是NA | |
| D. | 1molFeCl3跟沸水完全反应转化为氢氧化铁胶体,其中胶体粒子的数目是NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
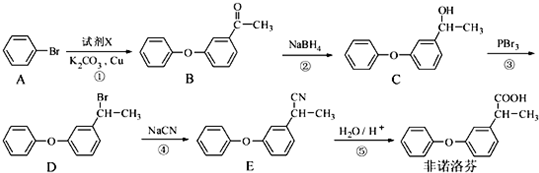
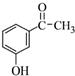 .
.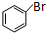 +2NaOH$\stackrel{一定条件}{→}$
+2NaOH$\stackrel{一定条件}{→}$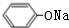 +NaBr+H2O.
+NaBr+H2O.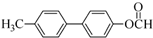 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
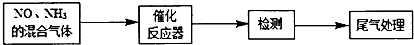
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 要检验某溴乙烷中的溴元素,可以加入NaOH溶液共热,冷却后滴入AgNO3溶液,观察有无浅黄色沉淀生成 | |
| B. | 用乙醇制取乙烯时所用温度计的位置与石油分馏时所用温度计的位置不同 | |
| C. | 用氨水清洗试管壁附着的银镜 | |
| D. | 制取乙炔时药品是电石和饱和食盐水,仪器用启普发生器 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3M(气)+2N(气)?P(气)+4Q(气) | B. | M(气)+2N(气)?3P(气)+Q(固) | ||
| C. | M(气)+N(气)?P(气) | D. | 以上都达到平衡 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com