
| A. | 晶体硅 | B. | 二氧化硅 | C. | 钢 | D. | 铝硅合金 |
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:选择题
| A. | Y位于第三周期,ⅦA族 | B. | 单质沸点:W>Y | ||
| C. | 气体氢化物稳定性:W>Z | D. | 离子半径:X<Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 今年1月12日,我国3名潜水员圆满完成首次300米饱和潜水作业,实现“下五洋
今年1月12日,我国3名潜水员圆满完成首次300米饱和潜水作业,实现“下五洋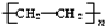 ;如图是贴在某垃圾桶上的标志,该标志的含义是可回收物.
;如图是贴在某垃圾桶上的标志,该标志的含义是可回收物.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
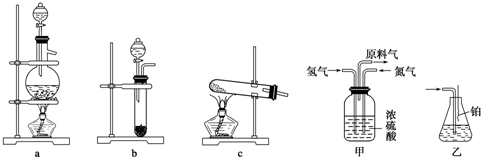
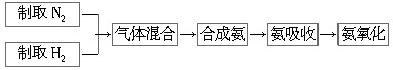
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
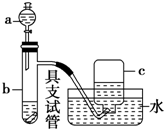 如图是用浓硝酸、铜片、水等试剂探究浓、稀硝酸的强氧化性并观察还原产物的实验装置.
如图是用浓硝酸、铜片、水等试剂探究浓、稀硝酸的强氧化性并观察还原产物的实验装置.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 厕所清洁剂、醋、肥皂、厨房清洁剂 | B. | 厕所清洁剂、厨房清洁剂、醋、肥皂 | ||
| C. | 醋、厕所清洁剂、肥皂、厨房清洁剂 | D. | 厨房清洁剂、醋、肥皂、厕所清洁剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3比Na2CO3热稳定性差 | |
| B. | NaHCO3比Na2CO3与稀盐酸反应的速度快 | |
| C. | 在相同温度下,Na2CO3的溶解度大于NaHCO3 | |
| D. | Na2CO3能使澄清石灰水变浑浊,而NaHCO3不行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5 | B. | 4 | C. | 3 | D. | 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com