
【题目】断裂1mol化学键所需要的能量如下:
化学键 | N-N | O=O | N≡N | N-H |
键能kJ·mol-1 | a | 500 | 942 | 391 |
肼(N2H4)的有关反应能量变化如图所示,下列说法正确的是( )

A. 该图表示:1molN2H4与1molO2反应生成1molN2和2molH2O反应热△H=-2752kJ·mol-1
B. a=154
C. N2(g)+2H2O(g)=N2H4(g)+O2(g) △H=+2752kJ·mol-1
D. 当有2molH2O(g)生成时,放出534kJ·mol-1的热量
【答案】B
【解析】
A. 反应热△H为生成物的总能量和反应物的总能量的差值,据图可知,1molN2H4(g)与1molO2(g)反应生成1molN2(g)和2molH2O(g)的反应热△H=-534kJ·mol-1,故A错误;
B. 据图可知N2H4(g)+O2(g)=2N(g)+4H(g)+2O(g) △H3=2752kJ/mol534kJ/mol=2218kJ/mol,化学键断裂吸收能量,化学键生成释放能量,断裂1molNN键所需的能量为a,则化学键断裂吸收的能量为:4×391+a+500=2218,解得a=154,故B正确;
C. 据图可知,N2(g)+2H2O(g)=N2H4(g)+O2(g) △H=+534kJ·mol-1,故C错误;
D. 据图可知,当有2molH2O(g)生成时,放出534kJ的热量,故D错误,答案选B。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】用蒸馏水稀释1mol/L氨水至0.01mol/L,随溶液的稀释,下列各项中始终保持增大趋势的是
A. c(OH-)/ c(NH3·H2O) B. c(NH![]() )/ c(OH-)
)/ c(OH-)
C. c(NH3·H2O)/ c(NH![]() ) D. c(OH-)
) D. c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列内容与结论相对应的是
选项 | 内容 | 结论 |
A | H2O(g)变成H2O(l) | △S>0 |
B | 硝酸铵溶于水可自发进行 | 因为△S>0 |
C | 一个反应的△H>0,△S>0 | 反应一定不自发进行 |
D | H2(g)+F2(g)=2HF(g),△H=-271kJ/mol △S=8J/(mol·K) | 反应在任意外界条件下均可自发进行 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组按下列路线合成医药中间体X和抗心律药盐酸阿齐利特:
I、
II、
已知:![]()
(1)下列说法不正确的是_____
A.A不能发生还原反应 B.X的分子式是C11H7ClO2
C.E→F的反应为取代反应 D.lmol盐酸阿齐利特最多与4molNaOH反应
(2)c 的化学方程式_____。
的化学方程式_____。
(3)D的结构简式_____。
(4)写出化合物B( C6H4ClNO2)符合条件的三种同分异构体的结构简式_____。
①1H﹣NMR谱表明分子中有4种氢原子,②IR谱显示有苯环、N=O键存在。
(5)![]() 可由 CH3CH2OH、CH3NH2等物质合成,请设计合成路线,无机试剂自选。__________
可由 CH3CH2OH、CH3NH2等物质合成,请设计合成路线,无机试剂自选。__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A(g)+B(s)![]() 3C(g)+4D(g)反应中,表示该反应速率最快的是
3C(g)+4D(g)反应中,表示该反应速率最快的是
A. v(A)=0.5 mol·L-1·s-1 B. v(B)=0.5 mol·L-1·s-1
C. v(C)=0.9mol·L-1·s-1 D. v(D)=1 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是 ( )
A.乙醛和丙烯醛(![]() )不是同系物,分别与氢气充分反应后的产物也不是同系物
)不是同系物,分别与氢气充分反应后的产物也不是同系物
B.O2与O3互为同素异形体,1H、2H、3H是氢元素的不同核素
C.C2H6O有两种同分异构体;2-甲基戊烷的结构简式为CH3CH2CH2CH(CH3)2
D.氨基酸分子中均含有羧基(—COOH)和氨基(—NH2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠-CO2电池的工作原理如图所示,吸收的CO2转化为Na2CO3固体和碳,沉积在多壁碳纳米管(MWCNT)电极表面,下列说法不正确的是( )
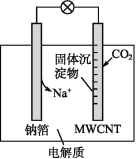
A.负极反应式为Na-e-=Na+
B.多壁碳纳米管(MWCNT)作电池的正极
C.可以用乙醇代替四甘醇二甲醚作有机溶剂
D.电池总反应式为4Na+3CO2=2Na2CO3+C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组为了研究外界条件对化学反应速率的影响,进行了酸性高锰酸钾与草酸的反应,记录以下实验数据:
实验编号 | 实验温度 | 试管中所加试剂及其用量 / mL | 溶液褪至无色所需时间/ min | |||
0.6mol/L H2C2O4 溶液 | H2O | 3mol/L H2SO4 稀溶液 | 0.05mol/L KMnO4溶液 | |||
① | 25 | 3.0 | V1 | 2.0 | 3.0 | 1.5 |
② | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
③ | 50 | 2.0 | V2 | 2.0 | 3.0 | 1.0 |
(1)请写出该反应的离子方程式__________________________________________,当该反应以表中数据反应完全时转移电子数为_______________NA
(2)V1 ______
(3)根据上表中的实验①、②数据,可以得到的结论是_____。
(4)探究温度对化学反应速率的影响,应选择_____(填实验编号)
(5)该小组同学根据经验绘制了 n (Mn 2+ )随时间变化的趋势如图 1 所示,但有同学查阅已有的实验资料发现,该实验过程中 n (Mn 2+ ) 随时间变化的实际趋势如图 2 所示。

该小组同学根据图 2 所示信息提出了新的假设,并设计以下实验方案继续进行实验探究。
实验编号 | 实验温度/℃ | 试管中所加试剂及其用量 | 再加入某种固体 | 溶液褪至无色所需时间 / min | |||
④ | 25 | 0.6mol/L H2C2O4 溶液 | H2O | 3mol/L H2SO4 稀溶液 | 0.05mol/L KMnO4 溶液 | ||
2.0 | 3.0 | 2.0 | 3.0 | MnSO4 | t | ||
①该小组同学提出的假设是_____。
②若该小组同学提出的假设成立,应观察到_________________________________现象。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组按下列路线合成甜味剂阿斯巴甜 :
:

已知:①芳香化合物A能发生银镜反应,核磁共振氢谱显示有5种不同化学环境的氢原子;
②
③RCN![]() RCOOH
RCOOH
④
回答下列问题:
(1)F的结构简式是_________________________________________。
(2)下列说法正确的是________。
A.化合物A的官能团是羟基
B.化合物B可发生消去反应
C.化合物C能发生加成反应
D.化合物D可发生加聚反应
(3)写出阿斯巴甜与足量NaOH水溶液充分反应的化学方程式:_________。
(4)写出同时符合下列条件的 D的同分异构体的结构简式:_________。
①有三种化学环境不同的氢原子;②含苯环的中性物质。
(5)参照上述合成路线,设计一条由甲醛为起始原料制备氨基乙酸的合成路线________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com