
| A�� | �٢ڢܢ� | B�� | �ۢܢݢ� | C�� | �ڢۢݢ� | D�� | �٢ڢݢ� |
���� �����ӿ�Ϊԭ�ӡ����ӣ���������ͬ�����ӿ���Ϊ��ԭ�����ӣ�
�ڻ�Ϊͬλ��ԭ�ӣ���������Ų���ͬ������������������ѧ���ʣ����������ʲ�һ����ͬ��
���������ӣ�������һ�������Ӵ��磬���ӵĵ�����һ������������һ�������Ӳ����磬���ӵ��������͵�����һ����ȣ��ݴ��жϣ�
����������ͬ��ԭ��Ϊͬ��Ԫ�أ�Ԫ�ص��о�������ԭ�ӣ�
��Ԫ�ز�̸��������һ��Ԫ�صIJ�ͬԭ���в�ͬ����������
��ԭ������������Ԫ��û����������
�ߢ�B�嵽��B�壬����7������͵ڢ����壻
���������Ų���ͬ��������ѧ���ʲ�һ����ͬ����Arԭ����S2-���ӣ�
��3517Cl��3717Cl��Ϊͬλ�أ���ѧ������ͬ��
��� �⣺����������ͬ�����Ӳ�һ������ͬ��Ԫ�ص�ԭ�ӣ��������������Ӻ���9�����ӣ���ԭ��Ҳ����9�����ӣ���������ͬ��Ԫ�ص�ԭ�ӣ��ʢٴ���
��Ԫ�ص�ԭ�ӵ�����������������Ԫ�����ʣ���ͬλ�ص�����������ȣ��������ǵĻ�ѧ���ʼ�����ȫ��ͬ�����������ʲ�һ����ͬ���ʢڴ���
�۷����Ե����ԣ����Ӵ��磬���������������͵���������ͬ�����һ��Ϊ���������������������ȣ�һ��Ϊ�������������͵���������ȣ�������������ì�ܣ����Բ�����Ϊһ�ַ��ӡ�һ�����ӣ��ʢ���ȷ��
�ܵ�������ͬ�����Ӳ�һ������ͬ��Ԫ�أ���CH4��H2O��Na+��Mg2+���ʢ���ȷ��
��һ��Ԫ�ؿ��ܴ��ڲ�ͬ�ĺ��أ�ͬһԪ�ص�ԭ�ӿ����в�ͬ�����������ʢݴ���
��Ԫ��û���������ĸ���ʢ���
�ߢ�B�嵽��B�壬����7������͵ڢ����壬�ڢ�����Ϊ8��9��10�������У���10�У�Ԫ�ض��ǽ���Ԫ�أ��ʢ���ȷ��
���������Ų���ͬ��������ѧ���ʲ�һ����ͬ����Arԭ�ӻ�ѧ�����ȶ�����S2-���Ӿ���ǿ��ԭ�ԣ��ʢ���ȷ��
��3517Cl��3717Cl��Ϊͬλ�أ���ѧ������ͬ���ʢ���ȷ��
��ѡ��D��
���� ������Ҫ����ѧ��������ԭ�ӵ���ϵ��ԭ�ӵĹ��ɼ����ӡ�ԭ�ӡ�����֮�����������ϵ��������Ƽ��ѶȲ�������֪ʶ��ȫ�棬��ѧ���ܴ��˼ά�ռ䣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ӿ�����������ܷⱣ�� | |
| B�� | ����������Һ�����ڴ���Ƥ���IJ����Լ�ƿ�� | |
| C�� | �������Ʊ������Ҵ��� | |
| D�� | ���Ƶ���ˮͨ����������ɫ�����Լ�ƿ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڼױ��м����������Ը��������Һ������ɫ����ȷ�Ľ��������ڲ����뱽�����Ӱ�죬ʹ�����ͱ������ױ����� | |
| B�� | �ú˴Ź���������1-������2-���� | |
| C�� | ����屽����һ�ֿռ�ṹ��֤���������в����ڵ�˫������Ľṹ | |
| D�� | 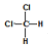 �� ��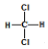 �� ��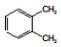 �� ��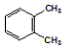 ����ͬ���칹�� ����ͬ���칹�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶��X��Y��W��Z | B�� | ԭ��������Y��X��Z��W | ||
| C�� | ԭ��������������Y��X��Z��W | D�� | ԭ�ӵĵ��Ӳ�����X=Y��W=Z |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
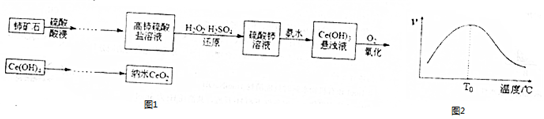
 ��ͼ��һ������ȼ�ϵ��װ��ʾ��ͼ���õ�������е����A��ϡ����Ϊ�������Һ�����������ṩ���ܣ������̵����ã����жԸõ�ص�˵������ȷ���ǣ�������
��ͼ��һ������ȼ�ϵ��װ��ʾ��ͼ���õ�������е����A��ϡ����Ϊ�������Һ�����������ṩ���ܣ������̵����ã����жԸõ�ص�˵������ȷ���ǣ�������| A�� | ͨ��H2�ĵ缫Ϊ������AΪNH4Cl | |
| B�� | ÿת��0.1mol���ӣ�����1.12L H2 | |
| C�� | ��Һ��H+��ͨ��N2��һ���ƶ���Cl-��ͨ��H2��һ���ƶ� | |
| D�� | ͨ��N2�ĵ缫�����ĵ缫��ӦʽΪN2+6e-+8H+�T2NH4+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | NaX |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 22.4 L��������е�̼ԭ����ĿΪ2NA | |
| B�� | �����£�0.2 mol Fe������ˮ������Ӧ�����ɵ�H2������ĿΪ0.3 NA | |
| C�� | ��NA��Na+��Na2O�ܽ���1 Lˮ�У�Na+�����ʵ���Ũ��Ϊ1 mol/L | |
| D�� | 5NH4NO3$\frac{\underline{\;\;��\;\;}}{\;}$2HNO3+4N2��+9H2O��Ӧ�У�����28 g N2ʱ��ת�Ƶĵ�����ĿΪ3.75NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com