
【题目】Na2SO3是一种白色粉末,工业上可用作还原剂、防腐剂等。某化学小组探究不同pH的Na2SO3溶液与同浓度AgNO3溶液反应的产物,进行如下实验。
实验Ⅰ 配制500 mL 一定浓度的Na2SO3溶液
①溶解:准确称取一定质量的Na2SO3晶体,用煮沸的蒸馏水溶解。蒸馏水需煮沸的原因是____
②移液:将上述溶解后的Na2SO3溶液在烧杯中冷却后转入仪器A中,则仪器A为 __,同时洗涤____(填仪器名称)2~3次,将洗涤液一并转入仪器A中;
③定容:加水至刻度线1~2 cm处,改用胶头滴管滴加蒸馏水至液面与刻度线相切,盖好瓶塞,反复上下颠倒,摇匀。
实验Ⅱ 探究不同pH的Na2SO3溶液与pH=4的AgNO3溶液反应的产物
查阅资料:i.Ag2SO3为白色固体,不溶于水,溶于过量Na2SO3溶液
ii.Ag2O,棕黑色固体,不溶于水,可与浓氨水反应
(1)将pH=8的Na2SO3溶液滴人pH=4的AgNO3溶液中,至产生白色沉淀。
假设一:该白色沉淀为Ag2SO3
假设二:该白色沉淀为Ag2SO4
假设三:该白色沉淀为Ag2SO3和Ag2SO4的混合物
①写出假设一的离子方程式 ____;
②提出假设二的可能依据是_____;
③验证假设三是否成立的实验操作是____。
(2)将pH=4的AgNO3溶液逐滴滴人足量的pH=11的Na2SO3溶液中,开始产生白色沉淀A,然后变成棕黑色物质。为了研究白色固体A的成分,取棕黑色固体进行如下实验:
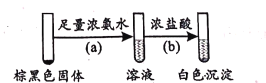
①已知反应(b)的化学方程式为Ag(NH3)2OH+3HCl=AgCl↓+2NH4Cl+H2O,则反应(a)的化学方程式为____;
②生成白色沉淀A的反应为非氧化还原反应,则A的主要成分是____(写化学式)。
(3)由上述实验可知,盐溶液间的反应存在多样性。经验证,(1)中实验假设一成立,则(2)中实验的产物不同于(1)实验的条件是 ___。
【答案】去除蒸馏水中的氧气,防止亚硫酸钠被氧化 500 mL容量瓶 烧杯、玻璃棒 SO32-+2Ag+= Ag2SO3 Na2SO3被酸化的NO3-氧化成Na2SO4,Na2SO4与AgNO3溶液反应生成Ag:2SO4沉淀 取固体少许加入足量 Na2SO3溶液(或向试管中继续滴加Na2SO3溶液) Ag2O + 4NH3·H2O =2Ag(NH3)2OH + 3H2O或Ag2O+4NH3+H2O=2Ag(NH3)2OH AgOH Na2SO3溶液滴加顺序不同 (或用量不同) ,溶液酸碱性不同(或浓度不同)
【解析】
配置一定物质的量浓度的溶液时,
①溶解时:Na2SO3晶体易被溶液中溶解的氧气氧化,故需煮沸;
②移液时:配置一定物质的量浓度的溶液时需要使用容量瓶,移液时需要洗涤烧杯和玻璃棒;
实验Ⅱ 探究不同pH的Na2SO3溶液与pH=4的AgNO3溶液反应的产物
①假设一是银离子与亚硫酸根离子反应生成亚硫酸银;
②考虑加入的酸性的硝酸银溶液具有氧化性,将亚硫酸银氧化成硫酸银;
③由于Ag2SO3溶于过量Na2SO3溶液,可以加入Na2SO3溶液验证溶液中是否有Ag2SO3;
(2) ① Ag2O为棕黑色固体,与氨水反应生成Ag(NH3)2OH和 3H2O;
②从非氧化还原反应分析得化合价不变,判断A的成分;
(3) (1)中实验和(2)中实验中溶液的滴加顺序不同,溶液酸碱性不同。
①溶解时:Na2SO3晶体易被溶液中溶解的氧气氧化,故需煮沸,防止亚硫酸钠被氧化;
②移液时:配置一定物质的量浓度的溶液时需要使用500ml的容量瓶,移液时需要洗涤烧杯和玻璃棒2~3次;
(1)①假设一是银离子与亚硫酸根离子反应生成亚硫酸银SO32-+2Ag+= Ag2SO3;
②将pH=8的Na2SO3溶液滴人pH=4的AgNO3溶液中,酸性溶液中存在氢离子,氢离子和硝酸根相当于硝酸,具有氧化性,可能会将亚硫酸根离子氧化成硫酸根;
③.Ag2SO3为白色固体,不溶于水,溶于过量Na2SO3溶液,故可以加入过量Na2SO3溶液,看是否继续溶解,若继续溶解一部分,说明假设三成立;
(2) ①Ag2O,棕黑色固体,不溶于水,可与浓氨水反应,反应a为Ag2O + 4NH3·H2O =2Ag(NH3)2OH + 3H2O;
②将pH=4的AgNO3溶液逐滴滴人足量的pH=11的Na2SO3溶液中,由于亚硫酸银易溶于亚硫酸钠,故生成的白色沉淀不是亚硫酸银,溶液呈碱性,也不是硫酸银,银离子在碱性条件下,例如银离子和氨水反应可以生成氢氧化银,是白色沉淀,A为AgOH;
(3)实验(1)将pH=8的Na2SO3溶液滴人pH=4的AgNO3溶液中,实验(2)将pH=4的AgNO3溶液逐滴滴人足量的pH=11的Na2SO3溶液中,对比两次实验可以看出,滴加顺序不同(或用量不同),,所给盐溶液酸碱性不同(或浓度不同)。


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案科目:高中化学 来源: 题型:
【题目】邮票是国家邮政发行的一种邮资凭证,被誉为国家名片。新中国化学题材邮票展现了我国化学的发展和成就,是我国化学史不可或缺的重要文献。下列说法错误的是
A. 邮票中的人物是侯德榜。其研究出了联产纯碱与氯化铵化肥的制碱新工艺,创立了中国人自己的制碱工艺一侯氏制碱法
邮票中的人物是侯德榜。其研究出了联产纯碱与氯化铵化肥的制碱新工艺,创立了中国人自己的制碱工艺一侯氏制碱法
B. 邮票中的图是用橡胶生产的机动车轮胎。塑料、橡胶和纤维被称为三大合成材料,它们不断替代金属成为现代社会使用的重要材料
邮票中的图是用橡胶生产的机动车轮胎。塑料、橡胶和纤维被称为三大合成材料,它们不断替代金属成为现代社会使用的重要材料
C. 邮票中的图是显微镜视野下的结晶牛胰岛素。我国首次合成的人工牛胰岛素属于蛋白质
邮票中的图是显微镜视野下的结晶牛胰岛素。我国首次合成的人工牛胰岛素属于蛋白质
D. 邮票是纪念众志成城抗击非典的邮票。冠状病毒其外壳为蛋白质,用紫外线、苯酚溶液、高温可以杀死病毒
邮票是纪念众志成城抗击非典的邮票。冠状病毒其外壳为蛋白质,用紫外线、苯酚溶液、高温可以杀死病毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2Cl2),非平面结构,常温下是一种黄红色液体,有刺激性恶臭,熔点80℃,沸点135.6℃,对干二氯化二硫叙述正确的是
A.二氯化二硫的电子式为![]()
B.分子中既有极性键又有非极性键
C.二氯化二硫属于非极性分子
D.分子中S-Cl键能小于S-S键的键能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。如图表示N2O在Pt2O+表面与CO反应转化成无害气体的过程。下列说法正确的是

A.N2O转化成无害气体时的催化剂是Pt2O2+
B.每1mol Pt2O+转化为Pt2O2+得电子数为3NA
C.将生成的CO2通人含大量SiO32-、Na+、Cl-的溶液中,无明显现象
D.1g CO2 、N2O的混合气体中含有电子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热△//=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△=2×(-57.3)kJ/mol
B.需要加热才能发生的反应一定是吸热反应
C.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的△H=+2×283.0kJ/mo1
D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.酸性碘化钾溶液中滴加适量双氧水:2I-+2H++H2O2=I2+2H2O
B.用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O
C.向苯酚钠溶液中通入少量CO2,溶液变浑浊:2![]() +CO2+H2O=2
+CO2+H2O=2![]() +CO32-
+CO32-
D.铅蓄电池充电时阴极反应式:PbSO42e-+2H2O=PbO2+SO42-+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合液25mL,向其中逐渐加入铁粉,产生气体的物质的量随铁粉质量增加的变化如图所示(硝酸的还原产物为NO,忽略反应中的溶液体积变化)。下列有关说法错误的是( )

A.OA段产生的气体是NO,AB段发生的反应为Fe+2Fe3+=3Fe2+,BC段产生的气体是H2
B.由此推断该条件下,氧化性:NO3-强于Fe3+
C.OA段与BC段产生的气体的体积比为1:1
D.C点溶质的物质的量浓度为10 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年10月1日是中华人民共和国成立 70 周年,国庆期间对大量盆栽鲜花施用了S-诱抗素制剂以保证鲜花盛开,利用如图所示的有机物X可生产S-诱抗素Y。下列说法不正确的是( )
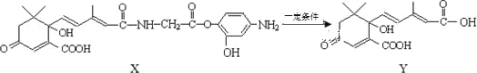
A.1mol Y 与足量 NaOH 溶液反应,最多消耗 2mol NaOH
B.Y 的分子式为 C15H19O6
C.1mol Y最多与 4mol H2 发生加成反应
D.X 可以发生氧化、取代、酯化、加聚、缩聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,![]() 与
与![]() 可发生反应:
可发生反应:![]() 下列关于R元素的叙述中,正确的是( )
下列关于R元素的叙述中,正确的是( )
A.R位于周期表中![]() 族B.R的气态氢化物的水溶液是强酸
族B.R的气态氢化物的水溶液是强酸
C.![]() 中的R只能被还原D.
中的R只能被还原D.![]() 在常温常压下一定是气体
在常温常压下一定是气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com