
| A. | 氯气通入石灰乳中,制取漂白粉 | |
| B. | 自来水厂可用明矾对水进行消毒杀菌 | |
| C. | 实验室保存氯化铁溶液时加少量盐酸,目的是防止Fe3+水解 | |
| D. | 常温下浓硝酸与铝、铁均不反应,可用铝或铁制的容器存放浓硝酸 |
分析 A.氯气与石灰乳制备漂白粉;
B.明矾不具有强氧化性;
C.Fe3+水解生成氢离子和氢氧化铁;
D.常温下浓硝酸与铝、铁发生钝化.
解答 解:A.氯气与石灰乳制备漂白粉,故A正确;
B.明矾不具有强氧化性,不能杀菌消毒,但水解生成胶体可除去水中悬浮杂质,故B错误;
C.Fe3+水解生成氢离子和氢氧化铁,所以实验室配制氯化铁溶液时通常需要加入盐酸,目的是抑制铁离子水解,故C正确;
D.常温下浓硝酸浓硝酸与铝、铁发生钝化,为氧化还原反应,生成致命的氧化膜阻止反应的进一步发生,故D错误;
故选AC.
点评 本题考查物质的性质,综合考查元素化合物,为高频考点,把握物质的性质及发生的反应为解答的关键,注意性质与用途的关系,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 有机溶剂(如乙醚、乙醇、苯、丙酮等)沸点低,极易被引燃,加热时最好用水浴加热 | |
| B. | 石油裂解、海水制镁、纤维素制火棉都包含化学变化 | |
| C. | 大分子化合物油脂在人体内水解为氨基酸和甘油等小分子才能被吸收 | |
| D. | 苹果放在空气中久置变黄和纸张久置变黄原理不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
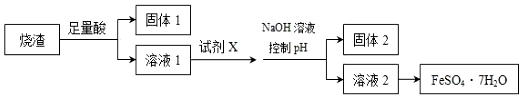
| A. | 溶解烧渣选用足量硫酸,试剂 X 选用铁粉 | |
| B. | 固体1 中一定含有 SiO2,控制 pH 是为了使 Al3+转化为 Al(OH)3,进入固体 2 | |
| C. | 从溶液 2 得到 FeSO4•7H2O 产品的过程中,须控制条件防止其氧化和分解 | |
| D. | 若改变方案,在溶液 1 中直接加 NaOH 至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到 FeSO4•7H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
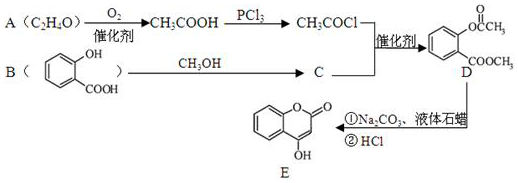
 .
.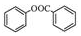 )的合成路线(无机原料任选).
)的合成路线(无机原料任选). .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙二醇和丙三醇互为同系物 | |
| B. | 醇都可以发生消去反应 | |
| C. | 醇在Cu催化作用下都可以催化氧化 | |
| D. | 饱和一元脂肪醇的化学式可用通式CnH2n+2O表示 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 催化剂能使不起反应的物质发生反应 | |
| B. | 催化剂在化学反应前后,化学性质和质量都不变 | |
| C. | 催化剂能改变化学反应速率 | |
| D. | 任何化学反应,都需要催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在任何条件下,化学平衡常数都是一个定值 | |
| B. | 当改变反应物的浓度时,化学平衡常数会发生改变 | |
| C. | 化学平衡常数K只与温度有关,与反应物浓度、体系的压强无关 | |
| D. | 化学平衡常数K可以推断一个可逆反应进行的程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 44.8 L氟化氢气体分解成22.4 L的氢气和22.4 L的氟气吸收546.6 kJ热量 | |
| B. | 1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量大于546.6 kJ | |
| C. | 相同条件下,1 mol氢气与1 mol氟气的能量总和高于2 mol氟化氢气体的能量 | |
| D. | 2 mol H-F键的键能比1 mol H-H键和1 mol F-F 键的键能之和大546.6 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
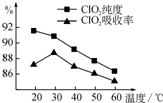 某研究小组用黄铁矿(FeS2)、氯酸钠和硫酸溶液混合反应制备ClO2气体,再用水吸收该气体可得ClO2溶液.在此过程中需要控制适宜的温度,若温度不当,副反应增加,影响生成ClO2气体的纯度,且会影响ClO2的吸收率,具体情况如图所示.
某研究小组用黄铁矿(FeS2)、氯酸钠和硫酸溶液混合反应制备ClO2气体,再用水吸收该气体可得ClO2溶液.在此过程中需要控制适宜的温度,若温度不当,副反应增加,影响生成ClO2气体的纯度,且会影响ClO2的吸收率,具体情况如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com