
【题目】硅烷是一种无色、与空气反应并会引起窒息的气体.其分子结构和![]() 相似,但
相似,但![]() 键键能比
键键能比![]() 键键能低。下列判断错误的是
键键能低。下列判断错误的是
A.![]() 分子呈正四面体形
分子呈正四面体形
B.![]() 分子是非极性分子
分子是非极性分子
C.因为![]() 键键能比
键键能比![]() 键键能低,所以
键键能低,所以![]() 沸点低于
沸点低于![]() 沸点
沸点
D.![]() 分子稳定性低于
分子稳定性低于![]() 分子,因为
分子,因为![]() 键键能高
键键能高
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下面两表分别列出了CO和![]() 的某些性质及相关键能,有关说法不正确的是
的某些性质及相关键能,有关说法不正确的是
表1:
分子 | 熔点 | 沸点 | 常温时在水 中溶解度 |
CO |
|
|
|
|
|
|
|
表2:
CO |
|
|
|
键能 |
|
| |
|
|
|
|
键能 | 193 | 418 | 946 |
A.CO与![]() 的价电子总数相等
的价电子总数相等
B.由表2可知,CO的活泼性不及![]()
C.由表1可知,CO的熔沸点高于![]() ,是因为CO分子间作用力大于
,是因为CO分子间作用力大于![]()
D.由表1可知,室温时,CO在水中的溶解性大于![]() ,是因为CO分子有弱极性
,是因为CO分子有弱极性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置或操作能达到实验目的的是

① ② ③ ④
A. 装置①可用于证明SO2与NaOH溶液发生了反应
B. 若装置②中X为CCl4,可用于吸收氨气或氯化氢
C. 装置③可用于实验室从食盐水中提取氯化钠
D. 装置④可用于证明溴乙烷与NaOH乙醇溶液共热生成乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面提到的问题中,与盐的水解无关的正确说法是
①明矾和FeCl3可作净水剂
②为保存FeCl3溶液,要在溶液中加少量盐酸
③AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是Al2O3
④NH4Cl与ZnCl2溶液可作焊接中的除锈剂
⑤实验室盛放Na2CO3、Na2SiO3等溶液的试剂瓶应用橡皮塞,而不能用玻璃塞
⑥用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂
⑦长期使用硫铵,土壤酸性增强;草木灰与铵态氮肥不能混合施用
A.①④⑦B.全有关C.②⑤D.③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。按图连接装置,用酒精灯对烧瓶B加热,当观察到D中有明显现象时停止实验。试完成下列问题:
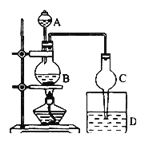
(1)浓硫酸的作用是________________。
(2)球形干燥管除起冷凝作用外,另一重要作用是___________。
(3)装置D中饱和碳酸钠溶液的作用是_____________。
(4)装置B中反应的化学方程式:_______。
(5)实验完成后利用________________方法分离出粗产品;粗产品往往含有少量的水,精制的方法是向粗产品中加入_________________后再利用_________________方法提纯。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO和![]() 的某些性质及相关键能如下表所示,下列说法不正确的是
的某些性质及相关键能如下表所示,下列说法不正确的是
表一
分子 | 熔点 | 沸点 | 常温时在水中的溶解度 |
CO |
|
|
|
|
|
|
|
表二
碳氮键 |
|
|
|
键能 |
|
|
|
氮氮键 |
|
|
|
键键能 | 193 | 418 | 946 |
A.CO与![]() 的价电子总数相等
的价电子总数相等
B.由表2可知,CO的活泼性不及![]() ,因为
,因为![]() 的键能大于
的键能大于![]()
C.由表1可知,CO的熔沸点高于![]() ,因为CO分子间作用力大于
,因为CO分子间作用力大于![]()
D.由表1可知,室温时CO在水中的溶解度大于![]() ,因为CO是极性分子
,因为CO是极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关使用的实验仪器及操作等说法正确的是( )
A.在分液实验中,待液体静置分层后,上、下层液体都应分别从分液漏斗下端的活塞放出
B.粗盐提纯中,可先加过量的Na2CO3溶液再加过量的BaCl2溶液来除去Ca2+和SO42-
C.利用蒸发浓缩冷却结晶的方法制备KNO3,对析出的KNO3晶体用酒精洗比用水洗好
D.制取蒸馏水的实验中,球形冷凝管的冷水应从下口进入,上口流出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,将足量的CaCO3固体分别加入同体积下列各溶液中,CaCO3溶解最少的是
A.1 mol·L-1的Na2CO3溶液B.2 mol·L-1的K2CO3溶液
C.2 mol·L-1的HCl溶液D.1 mol·L-1的NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氮及其化合物的转化很有意义。下面是氮的氧化物在几种不同情况下的转化:
①已知:2SO2(g)+O2(g)![]() 2SO3(g) H= -196.6 kJmol-1
2SO3(g) H= -196.6 kJmol-1
2NO(g)+O2(g)![]() 2NO2(g) H=-113.0kJmol-1
2NO2(g) H=-113.0kJmol-1
则SO2气体与NO2气体反应生成SO3气体和NO气体的热化学方程式为:______________。
②a.向绝热恒容密闭容器中通入SO2和NO2,一定条件下使其反应达到平衡,正反应速率随时间变化的示意图如图1所示。反应在c点________(“达到”或“未到”)平衡状态。
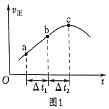
b.开始时,分别在该容器中加入Ⅰ:2mol SO2(g)和2 mol NO2(g)
Ⅱ:2 mol SO3(g)和2 mol NO(g)。则反应达到平衡时,比较容器Ⅰ和容器Ⅱ中反应平衡常数:Ⅰ____Ⅱ(填“>”“=”或“<”)。 .
(2)已知在温度为T时,CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1 molL-1,c始(H2O)=1 molL-1,某时刻经测定CO的转化率为10%,则该反应________(填“已经”或“没有”)达到平衡,原因是________。此时刻v正________v逆(填“>”或“<”)。 .
CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1 molL-1,c始(H2O)=1 molL-1,某时刻经测定CO的转化率为10%,则该反应________(填“已经”或“没有”)达到平衡,原因是________。此时刻v正________v逆(填“>”或“<”)。 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com