
| A. | 向正反应方向移动 | B. | 向逆反应方向移动 | ||
| C. | 平衡不发生移动 | D. | 不发生移动,但容器内压强增大 |
科目:高中化学 来源: 题型:解答题
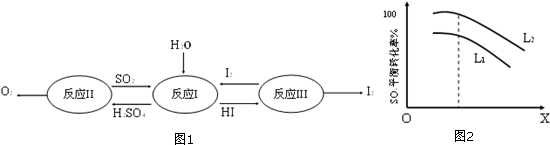
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某物质既能溶于盐酸,又能溶于NaOH溶液,则该物质一定是Al2O3 | |
| B. | 某气体只含C、H两种元素,且质量之比为6:1,则该气体一定为纯净物 | |
| C. | SO2通入品红溶液中,溶液褪色,则SO2通入紫色石蕊试液中,溶液也褪色 | |
| D. | 浓硝酸在光照条件下变黄,说明浓硝酸不稳定,生成的有色产物能溶于浓硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 X、Y、Z、W、Q五种元素的原子序数依次增大,X、Y、Z、W属于短周期元素.已知X位于周期表的s区,其原子中电子层数和未成对电子数相同;Y原子核外有三个能级,且每个能级上容纳的电子数相同;W原子最外层电子数是次外层电子数的3倍;Q元素的原子核外有26个运动状态完全不相同的电子.回答下列问题:
X、Y、Z、W、Q五种元素的原子序数依次增大,X、Y、Z、W属于短周期元素.已知X位于周期表的s区,其原子中电子层数和未成对电子数相同;Y原子核外有三个能级,且每个能级上容纳的电子数相同;W原子最外层电子数是次外层电子数的3倍;Q元素的原子核外有26个运动状态完全不相同的电子.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2(g)+Cl2(g)═2HCl(g)△H=-184.8KJ/mol | |
| B. | C2H4(g)+O2(g)═2CO2(g)+2H2O(l)△H=-1411.0KJ/mol | |
| C. | CH4(g)+$\frac{3}{2}$O2(g)═CO(g)+2H2O(l)△H=-6071.3KJ/mol | |
| D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8KJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用装置①分离碘并回收苯 | |
| B. | 用装置②灼烧海带灰 | |
| C. | 用装置③配置一定物质的量浓度的H2SO4溶液 | |
| D. | 用装置④蒸发浓缩MgCl2溶液制取MgCl2•6H2O晶体 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一上10月月考化学试卷(解析版) 题型:选择题
在一定条件下,某化合物X受热分解2X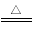 A↑+2B↑+4C↑,测得反应后生成的混合气体对H2的相对密度为11.43,在相同条件下,X的相对分子质量是
A↑+2B↑+4C↑,测得反应后生成的混合气体对H2的相对密度为11.43,在相同条件下,X的相对分子质量是
A.11.43 B.22.85 C.80.01 D.160.02
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:选择题
对于化学反应3W(g)+2X(g)=4Y(g)+3Z(g),下列反应速率关系中,正确的是
A.υ(W)=3υ(Z) B.2υ(X)=3υ(Z) C.2υ(X)=υ(Y) D.3υ(W)=2υ(X)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com