
下列说法正确的是 ( )
①参加反应的物质的性质是影响化学反应速率的主要因素
②光是影响某些化学反应速率的外界条件之一
③决定化学反应速率的主要因素是浓度
④不管什么反应,增大浓度,或加热或加压,或使用催化剂,都可以加快反应速率
A.①② B.②③
C.③④ D.①④
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
下列有关化学反应过程或实验现象的叙述中,正确的是
A.氯气的水溶液可以导电,说明氯气是电解质
B.漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的
C.氯气可以使湿润的有色布条褪色,但实际起漂白作用的物质是次氯酸而不是氯气
D.为证明氯水中含Cl-,可先加盐酸酸化,再加入AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2型分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g/L; W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
A.原子半径: W>Z>Y>X>M B.XZ2、X2M2、W2Z2均为直线形的共价化合物
C.由X元素形成的单质不一定是导体
D.由 X、Y、Z、M四种元素形成的化合物一定既含有离子键,又含有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
第三周期元素X,它的原子核外最外层实现8电子稳定结构所需电子数小于次外层和最内层的电子数之
差,且等于最内层电子数的整数倍.则下列说法正确的是( )
A.X元素最高价氧化物的水化物一定是强酸
B.X元素的氢化物的化学式一定为H2X
C.X元素在常温下稳定存在的氧化物一定能与烧碱反应
D.X的单质一定是良好的半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径(×10-10 m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
| 主要化合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | —— |
| 最低负价 | —— | -1 | —— | —— | -3 | -2 |
下列说法正确的是( )
A.元素X和Q形成的化合物中不可能含有共价键
B.X、Z、R的最高价氧化物的水化物之间可两两相互反应
C.R3-比Q2-更容易失去电子
D.M(OH)2的碱性比XOH的碱性强
查看答案和解析>>
科目:高中化学 来源: 题型:
某探究小组利用丙酮的溴代反应(CH3COCH3+Br2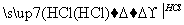 CH3COCH2Br+HBr)来研究反
CH3COCH2Br+HBr)来研究反
应物浓度与反应速率的关系.反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定.在一定温度下,获得如下实验数据:
| 实验 | 初始浓度c/mol/L | 溴颜色消失所需时间t/s | ||
| 序号 | CH3COCH3 | HCl | Br2 | |
| ① ② ③ ④ | 0.80 1.60
0.80 | 0.20 0.20 0.40 0.20 | 0.0010 0.0010 0.0010 0.0020 | 290 145
580 |
分析实验数据所得出的结论不正确的是 ( )
A.增大c(CH3COCH3),v(Br2)增大
B.实验②和③的v(Br2)相等
C.增大c(HCl),v(Br2)增大
D.增大c(Br2),v(Br2)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
加入0.1 mol的MnO2粉末于50 mL过氧化氢的溶液中(密度为1.1 g·mL-1),在标准状况下放出气体的体积和时间的关系如右图所示,回答下列问题:
(1)A、B、C、D四点化学反应速率快慢的顺序为________。
(2)解释反应速率变化的原因______________________________
____________________________________________________________________。
(3)计算过氧化氢的初始物质的量浓度___________________________________。
(4)求反应进行到2分钟时过氧化氢的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组探究SO2和Fe(NO3)3溶液的反应,其反应装置如下图所示:
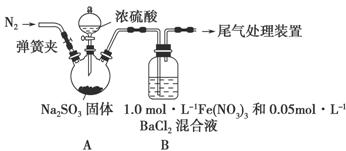
已知:1.0 mol·L-1的Fe(NO3)3溶液的pH=1,请回答下列问题:
(1)装置A中反应的化学方程式是 。
(2)为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是
。
(3)装置B中产生了白色沉淀,其成分是 ,说明SO2具有 性。
(4)分析B中产生白色沉淀的原因:
猜想1: ;
猜想2:SO2与Fe3+反应;
猜想3:在酸性条件下SO2与NO3—反应;
①按猜想2,装置B中反应的离子方程式是 。
②按猜想3,只需将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验。应选择的试剂是 (填字母)。
a.0.1 mol·L-1硝酸钠溶液 b.1.5 mol·L-1Fe(NO3)2溶液
c.6.0 mol·L-1 NaNO3和0.2 mol·L-1盐酸等体积混合的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
有关石油的分馏和煤的干馏两种变化,下列叙述错误的是 ( )
A.加热的温度二者不同
B.获得的产品二者不同
C.前者是物理变化,后者是化学变化
D.前者不需要隔绝空气,后者需隔绝空气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com