
(本题共12分)已知: (X为卤原子,M为烃基或含酯基的取代基等)
(X为卤原子,M为烃基或含酯基的取代基等)
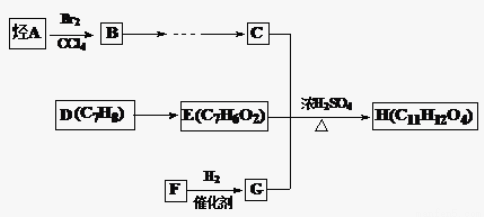
由有机物A合成G(香豆素)的步骤如下:

回答下列问题:
47.写出反应C+D→E的反应类型 。
48.A中官能团名称为 ;写出反应条件:E→F 。
49.写出结构简式:B ,D 。
50.F有多种同分异构体,写出同时满足下列条件的任意两种同分异构体的结构简式: 。
① 分子中除苯环外,无其它环状结构;
② 分子中有四种不同化学环境的氢原子;
③ 能发生水解反应,不能与金属钠反应;
④ 能与新制Cu(OH)2按物质的量之比1:2反应。
51.二氢香豆素( )常用作香豆素的替代品。鉴别二氢香豆素和它的一种同分异构体(
)常用作香豆素的替代品。鉴别二氢香豆素和它的一种同分异构体( )需要用到的试剂有:NaOH溶液、 。
)需要用到的试剂有:NaOH溶液、 。
52.已知: (R,R′为烃基)。试写出以苯和丙烯(
(R,R′为烃基)。试写出以苯和丙烯( =CH—CH3)为原料,合成
=CH—CH3)为原料,合成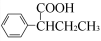 的路线流程图(无机试剂任选)。合成路线流程图示例如下:
的路线流程图(无机试剂任选)。合成路线流程图示例如下:

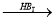
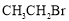

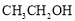

47、取代 (1分) 48、碳碳双键、醛基 (0.5分×2);NaOH溶液/加热(1分)、 H+(硫酸或盐酸)(1分)49、CH2=CHCHO;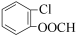 (1分×2)
(1分×2)
50、 、
、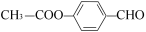 (合理即可)(1分×2)
(合理即可)(1分×2)
51、 稀硫酸、FeCl3溶液(或稀硫酸、溴水等)(0.5分×2)
52、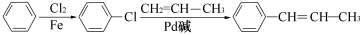
 (合理即可)(1分×3)
(合理即可)(1分×3)
【解析】
试题分析:A能发生银镜反应,则根据A的分子式可知A的结构简式为CH2=CHCHO,B的结构简式为CH2=CHCOOH。B与甲醇发生酯化反应生成C,则C的结构简式为CH2=CHCOOCH3。根据已知信息可知C与D生成E的反应应该是D中苯环上的氯原子被取代,则根据E的结构简式可知D的结构简式为 。根据F的分子式可知E生成F的反应应该是酯基的水解反应,则F的结构简式为
。根据F的分子式可知E生成F的反应应该是酯基的水解反应,则F的结构简式为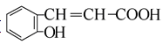 ,F分子分子内的酯化反应生成G。
,F分子分子内的酯化反应生成G。
47、根据以上分析可知反应C+D→E的反应类型是取代反应;
48、根据A的结构简式可知A中官能团名称为碳碳双键、醛基;E生成F是酯基的水解反应,则反应条件是NaOH溶液/加热然后加入H+(硫酸或盐酸)酸化即可;
49、根据以上分析可知B、D的结构简式分别是CH2=CHCHO、 ;
;
50、①分子中除苯环外,无其它环状结构;②分子中有四种不同化学环境的氢原子,即含有4类等效氢原子;③能发生水解反应,不能与金属钠反应,说明含有酯基,不存在羟基;④能与新制Cu(OH)2按物质的量之比1:2反应,说明含有1个醛基,因此满足条件的有机物结构简式为 、
、 ;
;
51、根据有机物的结构简式可知二者含有相同的官能团酯基,但酯基水解后的羟基不同,前者是酚羟基,后者是醇羟基,据此可以检验,因此所用试剂为稀硫酸、FeCl3溶液(或稀硫酸、溴水等);
52、根据已知信息并依据最终产品的结构简式可依据逆推法进行分析,即要合成该产品,需要 ,羟基可以通过碳碳双键与水加成得到,再根据题中信息苯环上的氯原子可以被烯烃基取代,所用合成路线可以设计为
,羟基可以通过碳碳双键与水加成得到,再根据题中信息苯环上的氯原子可以被烯烃基取代,所用合成路线可以设计为
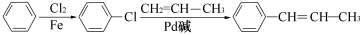
 。
。
考点:考查有机合成与制备、官能团、同分异构体、反应条件、有机反应类型以及方程式书写等


科目:高中化学 来源:2014-2015学年浙江省高三1月份阶段测试化学试卷(解析版) 题型:选择题
2013年6月20日,中国首次太空授课活动成功举行,神舟十号航天员王亚平在天宫一号展示了失重环境下的物理现象。若在天宫一号中进行以下实验,其中最难完成的是
A.将金粉和铜粉混合 B.将牛奶加入水中混合
C.蒸发食盐水制取食盐晶体 D.用漏斗、滤纸过滤除去水中的泥沙
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闸北区高三上学期期末化学试卷(解析版) 题型:填空题
(本题共14分)碘海醇为非离子型造影剂,尤适用于有造影剂反应的高危因素的病人。
下面是以化合物A为原料合成碘海醇的路线:
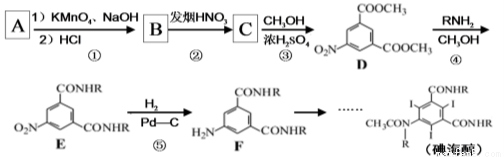
其中R-为-CH2CH(OH)CH2OH
请回答以下问题:
48.碘海醇的分子式为________。
49.A是苯的同系物,其蒸气相对氢气的密度是53,则A的结构简式是 。
50.写出A的侧链与氯气发生一氯取代的条件_____________。
51.反应①→⑤中,属于取代反应的是_____________(填序号)。
52.写出能同时满足下列条件的D的两种同分异构体的结构简式:________。
Ⅰ.苯环上有3个取代基,苯环上的一卤代物有2种;
Ⅱ.能发生银镜反应,水解产物之一能与FeCl3溶液发生显色反应;
Ⅲ.含有1个α-氨基酸的结构(例如: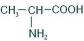 属于α-氨基酸);
属于α-氨基酸);
53.已知:①
②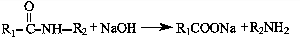
③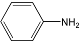 呈弱碱性,易被氧化
呈弱碱性,易被氧化
请写出以 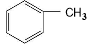 和(CH3CO)2O为原料制备染料中间体
和(CH3CO)2O为原料制备染料中间体 的合成路线流程图(无机试剂任用)。
的合成路线流程图(无机试剂任用)。
(合成路线常用的表示方式为: )
)
__________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闸北区高三上学期期末化学试卷(解析版) 题型:选择题
将40℃的饱和硫酸铜溶液升温至50℃,或者温度仍保持在40℃而加入少量无水硫酸铜,在这两种情况下均保持不变的是
A.硫酸铜的溶解度 B.溶液的质量
C.溶液中溶质的质量分数 D.溶液中Cu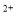 的数目
的数目
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闸北区高三上学期期末化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.摩尔是可以把物质的质量与微观粒子数联系起来的一个基本物理量
B.0.012 kg 12C中所含的碳原子数为NA
C.物质的摩尔质量等于其相对分子(原子)质量
D.1mol任何物质都含有约6.02×1023个原子
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市普陀区高三一模化学试卷(解析版) 题型:填空题
(本题共12分)氨是一种重要的化工产品。“一氧化碳变换”是合成氨原料气生产中的重要环节,其反应方程式为:CO(g) + H2O(g) CO2(g) + H2(g)
CO2(g) + H2(g)
完成下列填空:
23.恒温恒容条件下,能说明该反应达到平衡状态的是 (填字母序号)。
a.ν(CO)消耗 = ν(H2O)生成 b.c(CO2) = c(CO)
c.混合气体的总压不再改变 d.混合气体的密度不再改变
24.将不同量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中进行反应,得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
CO | H2O | CO2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 5 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
3 | 650 | 2 | 1 | A | B | t |
①实验1中从反应开始到达到平衡,以H2的浓度变化表示的反应速率为 。
②A = 。
③平衡常数:K(900℃) K(650℃) (填“>”、“<”或“=”=)。
25.温度是一氧化碳变换中最重要的工艺条件,实际生产过程中将温度控制在400℃左右,可能的原因是 。
26.C、H、O、N元素中,核外电子占据5个不同轨道的原子,其最外层电子排布式是 。这四种元素形成的化合物 (填“一定是”、“一定不是”、“不一定是”)离子化合物。
27.能证明碳的非金属性比硅强的事实是 (选填编号)。
a.酸性:H2CO3强于H2SiO3 b.高温下SiO2与C生成Si和CO
c.键的极性:C-H > Si-H d.熔点:金刚石 > 单晶硅
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市普陀区高三一模化学试卷(解析版) 题型:选择题
芳炔类大环化合物是新兴的一种富碳共轭大环状分子。苯乙炔(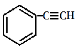 )可用于合成一系列芳炔类大环化合物,其结构如下。有关叙述正确的是
)可用于合成一系列芳炔类大环化合物,其结构如下。有关叙述正确的是

A.上述四种物质属于苯乙炔的同系物
B.第一种物质的分子式为C18H12
C.它们可通过苯乙炔的加成反应获得
D.该系列化合物的含碳量均相同
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市嘉定区高三一模化学试卷(解析版) 题型:填空题
某芳香族化合物H(C11H12O4)是有机合成工业的一种重要的中间产物,其合成路线如下。已知2molC分子可缩合生成1mol六元环化合物分子。F常温下是气体,水溶液具有很好的防腐杀菌效果,且能与新制氢氧化铜反应。请回答下列问题:
49.F的电子式为 , A的结构简式
B转化为C的条件是
A.水解、酸化、氧化、还原 B.氧化、水解、酸化、还原
C.水解、酸化、还原、氧化 D.氧化、酸化、水解、还原
50.以C为原料可合成可降解塑料,试写出其化学方程式
51.H与氢氧化钠溶液反应的化学方程式
52.H的同分异构体有多种,请写出符合下列条件的同分异构体的结构简式
。(写两种即可)
①苯环上只有两个取代基,苯环上的一氯取代物只有两种
②1mol的H与足量的NaHCO3溶液反应,生成2molCO2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市虹口区高三上学期期末考试化学试卷(解析版) 题型:选择题
根据右表,以下错误的是
酸 | HF | H3PO4 |
电离常数 | Ki = 3.6×10 - 4 | Ki1= 7.5×10 -3 Ki2= 6.2×10 -8 Ki3= 2.2×10 -13 |
A.NaF和H3PO4反应的产物只有HF、NaH2PO4
B.0.10 mol/L的溶液,pH由大到小的顺序是Na3PO4>Na2HPO4>NaF>NaH2PO4
C.0.10 mol/L的H3PO4溶液中,0.30 mol/L>c(H+)>0.10 mol/L
D.25℃时,等体积、等浓度的NaF和NaH2PO4溶液中所含离子总数前者小于后者
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com