
| A. | C(s)+$\frac{1}{2}$O2(g)=CO(g);△H=-393.5 kJ/mol | |
| B. | 2H2(g)+O2(g)=2H2O(g);△H=+571.6 kJ/mol | |
| C. | CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890.3 kJ | |
| D. | $\frac{1}{2}$C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l);△H=-1400 kJ/mol |
分析 燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量,根据燃烧热的定义判断热化学方程式是否正确.
解答 解:A.C完全燃烧应生成CO2,生成CO,反应热小于393.5kJ/mol,故A错误;
B.H2完全燃烧生成的稳定的氧化物为液态水,故B错误;
C.CH4完全燃烧生成稳定的氧化物为CO2和液态水,但焓变单位错误,故C错误;
D.1mol葡萄糖完全燃烧生成CO2和H2O(l),燃烧热为2800kJ/mol,则$\frac{1}{2}$mol葡萄糖完全燃烧放出1400kJ热量,故D正确;
故选D.
点评 本题考查热化学方程式,题目难度不大,本题注意把握燃烧热的概念,特别是水,稳定状态为液态.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 胆矾、漂白粉、氯化钾、硫酸钡 | B. | 盐酸、空气、硝酸、干冰 | ||
| C. | 冰醋酸、海水、氧化铝、乙醇 | D. | 蛋白质、油脂、烧碱、石灰石 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v正(CH3OH)=v正(CO2) | B. | 混合气体的密度不变 | ||
| C. | c(CH3OH)=c(H2O) | D. | 混合气体的总物质的量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑥ | B. | ①③⑥⑦ | C. | ②④⑤⑧ | D. | ②⑤⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ①③④⑤ | C. | ①③⑤ | D. | ①②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu→Cu(OH)2 | B. | CaCl2→CaO | C. | Fe2O3→Fe | D. | Cu(NO3)2→AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 材料的不断发展可以促进社会进步.
材料的不断发展可以促进社会进步.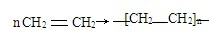 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com