
| A、FeO |
| B、Fe2O3 |
| C、FeSO4 |
| D、Fe3O4 |
| m |
| 72 |
| m |
| 152 |
| m |
| 232 |


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
| A、1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA |
| B、0.1mol丙烯酸中含有双键的数目为0.1NA |
| C、标准状况下,11.2L苯中含有分子的数目为0.5NA |
| D、在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
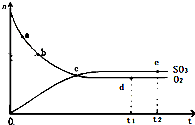 对于密闭容器中的反应:2SO2(g)+O2(g)?2SO3(g)△H<0,450℃时,n(SO3)和n(O2)随时间的变化关系如图所示,下列说法正确的是( )
对于密闭容器中的反应:2SO2(g)+O2(g)?2SO3(g)△H<0,450℃时,n(SO3)和n(O2)随时间的变化关系如图所示,下列说法正确的是( )| A、点c处反应达到平衡 |
| B、点a的正反应速率比点b的大 |
| C、点d(t1时刻)和点e(t2时刻)处n(SO2)不一样 |
| D、其他条件不变,600℃时反应至t1时刻,n(SO3)比上图中的d点值要大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、全部 | B、①②③④⑤ |
| C、③④⑤⑥ | D、①②⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 氢氧化钠溶液 | 分液 |
| B | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| C | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 蒸馏 |
| D | 乙炔(硫化氢) | 硫酸铜 | 洗气 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
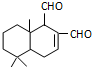 某天然拒食素具有防御非洲大群蚯蚓的作用,其结构简式如图(未表示出原子或原子团的空间排列).该拒食素与下列某试剂充分反应,所得有机物分子的官能团数目增加,则该试剂是( )
某天然拒食素具有防御非洲大群蚯蚓的作用,其结构简式如图(未表示出原子或原子团的空间排列).该拒食素与下列某试剂充分反应,所得有机物分子的官能团数目增加,则该试剂是( )| A、Br2的CCl4溶液 |
| B、Ag(NH3)2OH溶液 |
| C、HBr |
| D、H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子中C、H、O个数之比为1:4:4 |
| B、分子中C、H个数之比为1:2 |
| C、分子中可能含有氧原子 |
| D、此有机物的最简式为CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
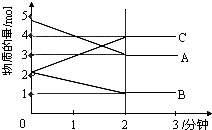 (1)写出该密闭容器发生反应的化学方程式为
(1)写出该密闭容器发生反应的化学方程式为查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com