
| A£® | NaCl | B£® | FeCl2 | C£® | FeCl3 | D£® | CuCl2 |
·ÖĪö ĀČĘų¾ßÓŠĒæµÄŃõ»ÆŠŌ£¬Óė±ä¼Ū½šŹō·“Ӧɜ³Éøß¼ŪĢ¬ĀČ»ÆĪļ£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗA£®ĀČĘųÓėÄĘ·“Ӧɜ³ÉĀČ»ÆÄĘ£¬¹ŹAÕżČ·£»
B£®ĢśÓėĀČĘų·“Ӧɜ³ÉĀČ»ÆĢś£¬¹ŹB“ķĪó£»
C£®ĢśÓėĀČĘų·“Ӧɜ³ÉĀČ»ÆĢś£¬¹ŹCÕżČ·£»
D£®ĶÓėĀČĘų·“Ӧɜ³ÉĀČ»ÆĶ£¬¹ŹDÕżČ·£»
¹ŹŃ”£ŗB£®
µćĘĄ ±¾Ģāæ¼²éĮĖĀČĘųµÄŠŌÖŹ£¬ŹģĻ¤ĀČĘųµÄĒæµÄŃõ»ÆŠŌŹĒ½āĢā¹Ų¼ü£¬×¢ŅāÓėĀČĘų±ä¼Ū½šŹō·“Ӧɜ³Éøß¼ŪĢ¬ĀČ»ÆĪļ£¬ĢāÄæÄŃ¶Č²»“ó£®


 ŌõѳѧŗĆÅ£½ņÓ¢ÓļĻµĮŠ“š°ø
ŌõѳѧŗĆÅ£½ņÓ¢ÓļĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚCl2ÖŠµćČ¼ĢśĖ棬ӊFeCl2Éś³É | |
| B£® | ŹµŃéŹŅĄūÓĆ·ĻĶŠ¼ÖĘČ”CuSO4ČÜŅŗµÄ×īŗƵķ½·ØŹĒ½«ĶŠ¼ŌŚæÕĘųÖŠ×ĘÉÕŗóŌŁČÜÓŚĻ”H2SO4 | |
| C£® | Š”ĖÕ“ņµÄÖ÷ŅŖ³É·ÖŹĒĢ¼ĖįÄĘ | |
| D£® | ŹµŃéŹŅÓĆĀČ»Æļ§ČÜŅŗŗĶĒāŃõ»ÆøĘČÜŅŗ»ģŗĻÖĘČ”°±Ęų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ńõ»Æ¼Į¾ßÓŠŃõ»ÆŠŌ£¬»¹Ō¼Į¾ßÓŠ»¹ŌŠŌ | |
| B£® | Ńõ»Æ¼ĮŌŚ·“Ó¦ÖŠŹ§Č„µē×Ó£¬»¹Ō¼ĮŌŚ·“Ó¦ÖŠµĆµ½µē×Ó | |
| C£® | ½šŹōŌŚ·“Ó¦ÖŠÖ»ÄÜ×÷»¹Ō¼Į£¬·Ē½šŹōŌŚ·“Ó¦ÖŠÖ»ÄÜ×÷Ńõ»Æ¼Į | |
| D£® | ŃōĄė×ÓÖ»ÓŠŃõ»ÆŠŌ£¬ŅõĄė×ÓÖ»ÓŠ»¹ŌŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® |  | ||
| C£® |  | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | K+”¢Fe3+”¢SCN-”¢Cl- | B£® | Fe3+”¢K+”¢OH-”¢SO42- | ||
| C£® | Fe2+”¢K+”¢Cl-”¢SO42- | D£® | Na+”¢H+”¢SO42-”¢CO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·ÅČȵķ“Ó¦·¢ÉśŹ±²»±Ų¼ÓČČ | |
| B£® | »Æѧ·“Ó¦Ņ»¶ØÓŠÄÜĮæ±ä»Æ | |
| C£® | ĪüČČ·“Ó¦Ņ»¶ØŠčŅŖ¼ÓČČŗó²ÅÄÜ·¢Éś | |
| D£® | »Æѧ·“Ó¦ČČŠ§Ó¦ŹżÖµÓė·“Ó¦ĪļÖŹ¶ąÉŁĪŽ¹Ų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2L0.5mol/LµÄŃĒĮņĖįČÜŅŗÖŠŗ¬ÓŠµÄH+Ąė×ÓŹżĪŖ2NA | |
| B£® | 2.0 gH218OŗĶD2OµÄ»ģŗĻĪļÖŠĖłŗ¬ÖŠ×ÓŹżĪŖNA | |
| C£® | µē½ā¾«Į¶ĶŹ±£®ČōŃō¼«ÖŹ×ī¼õÉŁ64g£¬ŌņŅõ¼«µĆµ½µÄµē×ÓŹżĪŖ2NA | |
| D£® | 1L 0.1 mol/LµÄNaHCO3ČÜŅŗÖŠHCO3-ÓėCO32-µÄĄė×ÓŹżĪŖ0£®l NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā


²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
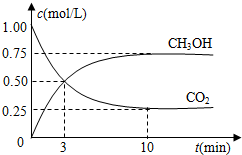
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com