
【题目】50mL 0.50molL﹣1盐酸与50mL 0.55molL﹣1NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.试回答下列问题: 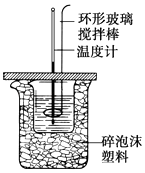
(1)大烧杯上如不盖硬纸板,求得的中和热数值将(填“偏大”、“偏小”或“无影响”).结合日常生活的实际该实验在中进行效果更好.
(2)实验中改用60m L 0.50molL﹣1盐酸与 50m L 0.55molL﹣1 NaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等”或“不相等”),所求中和热(填“相等”或“不相等”),简述理由 .
(3)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会;用50m L 0.5molL﹣1 NaOH溶液进行上述实验,测得的中和热的数值会 . (均填“偏大”、“偏小”或“无影响”)
【答案】
(1)偏小;保温杯
(2)不相等;相等;中和热是在稀溶液中,1molH+和1molOH﹣发生中和反应生成1molH2O时所放出的热量,与酸碱的用量无关
(3)偏小;偏小
【解析】解:(1)如不盖硬纸板,热量散失,不能准确测定最高温度,则求得的中和热数值将偏小,结合日常生活的实际该实验在保温杯中进行效果更好,
所以答案是:偏小;保温杯;(2)改用60m L 0.50molL﹣1盐酸与 50m L 0.55molL﹣1 NaOH溶液进行反应,生成水更多,放出的热量对,但中和热不变,因中和热是在稀溶液中,1 mol H+和1 mol OH﹣发生中和反应生成1 mol H2O时所放出的热量,与酸碱的用量无关,
所以答案是:不相等;相等;因中和热是在稀溶液中,1 mol H+和1 mol OH﹣发生中和反应生成1 mol H2O时所放出的热量,与酸碱的用量无关;(3)一水合氨电离吸热,则用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会偏小;用50m L 0.5molL﹣1 NaOH溶液进行上述实验,HCl不能完全反应,测得的中和热的数值会偏小,所以答案是:偏小;偏小.


科目:高中化学 来源: 题型:
【题目】科学家经过研究后发现,把水加热加压到 374℃、22.lMPa以上时具有很多特性, 如其中含有的氢离子浓度远远大于10-7mol/L,还具有很强的溶解有机物的能力。由此可知,处于这种状态下的水( )
A.显中性, pH一定等于 7B.表现出非极性溶剂的特性
C.显酸性,pH 一定小于 7D.表现出极性溶剂的特性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在给定条件下能大量共存的是( )
A. 在无色透明溶液中:Fe2+、K+、NO3-、Cl-
B. 在SO42-存在的溶液中:Na+、Mg2+、Ca2+、I-
C. 在PH=1的溶液中:K+、Ba2+、HCO3-、Br-
D. 在滴加酚酞试液显红色的溶液中:Na+、S2-、CO32-、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法中正确的是( )
A. 36.5g HCl所含的分子数为NAB. 22.4L H2O所含的分子数为NA
C. NA个氢原子的质量为2gD. 1 mol NaCl中含0.5NA个Na+和0.5NA个Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同温度下,0.01molL﹣1 NaOH溶液和0.01molL﹣1的盐酸相比,下列说法正确的是( )
A.由水电离出的[H+]相等
B.由水电离出的[H+]都是1.0×10﹣12 molL﹣1
C.由水电离出的[OH﹣]都是0.01 molL﹣1
D.两者都促进了水的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、NO的混合气体,这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中逐滴加入60 mL NaOH溶液至Cu2+恰好完全沉淀,则NaOH溶液的浓度是
A. 3 mol·L-1 B. 4 mol·L-1
C. 5 mol·L-1 D. 6 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 1 mol氢约含有6.02×1023个微粒
B. 1 mol H2O中含有的氢原子数为2NA
C. 钠的摩尔质量等于它的相对原子质量
D. 1 mol硫酸的质量等于98 g/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《礼记内则》中记载“冠带垢,和灰(草木灰)请漱;衣带垢,和灰请浣。”下列说法不正确的是( )
A.文中叙述涉及到水解反应B.“冠带垢,和灰请漱”有甘油生成
C.文中“灰”主要为NaOHD.文中“垢”成分还有油脂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com