
【化学—选修3:物质结构与性质】我国科学家借助自主研制的新型钨钴合金催化剂攻克了单壁碳纳米管结构的可控制备难题。
(1)基态钴原子的核外电子排布式为 。单壁碳纳米管可看作石墨烯沿一定方向卷曲而成的空心圆柱体,其碳原子的杂化方式为 。
(2)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化,已知甲醛各原子均满足稳定结构,甲醛分子属 分子(选填“极性”“非极性”),其立体构型为 。
(3)橙红色晶体羰基钴[Co2(CO)8]的熔点为52℃,可溶于多数有机溶剂。该晶体属于 晶体,三种元素电负性由大到小的顺序为(填元素符号) 。配体CO中σ键与π键数之比是 。
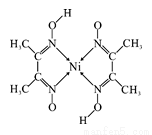
(4)元素铁、钴、镍并称铁系元素,性质具有相似性。某含镍化合物结构如上图所示,分子内的作用力不可能含有 (填序号)。
A离子键 B共价键 C金属键 D配位键 E氢键
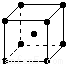
(5)钨为熔点最高的金属,硬度极大,其晶胞结构如图所示,已知钨的密度为ρ g·cm-3,则每个钨原子的半径r= cm。(只需列出计算式)
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源:2016-2017学年广西省高二上模拟考试化学卷(解析版) 题型:推断题
中学化学中几种常见物质的转化关系如图所示:

将D溶液滴入沸水中可得到以F为分散质的红褐色胶体.请回答下列问题:
(1)红褐色胶体中F粒子直径大小的范围:_______________.
(2) 写出A、B、H的化学式_____________、___________、_________________.
(3)①H2O2分子的电子式为______________.
②写出C的酸性溶液与双氧水反应的离子方 程式:_____________________________.
程式:_____________________________.
(4)鉴定E中阳离子时,可先加入_____________溶液,再加热使之产生气体
(5)在C溶液中加入与C等物质的量的Na2O2,恰好使C转化为F,写出该反应的离子方程式:________.
查看答案和解析>>
科目:高中化学 来源:2017届四川省绵阳市高三第二次诊断性考试化学试卷(解析版) 题型:实验题
碱式碳酸铜可用于有机催化剂、杀虫剂及饲料中铜的添加剂,还可用于烟火和颜料制造。CuSO4溶液与Na2CO3溶液反应能否得到碱式碳酸铜?某班同学进行相关探究。
【沉淀制备】
称取12.5 g胆矾溶于87.4 mL蒸馏水中,滴4滴稀硫酸,充分搅拌后得到CuSO4溶液。向其中加入适量Na2CO3溶液,将所得蓝绿色悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤。
(1)滴加稀硫酸的作用是 。所得硫酸铜溶液的溶质质量分数为 。
(2)用无水乙醇洗涤的目的是 。
【实验探究】
同学们设计了如下装置,用制得的蓝绿色固体进行实验:
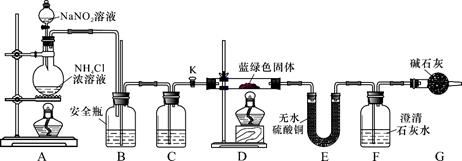
(3)D装置加热前,需要首先打开活塞K,用A装置制取适量N2,然后关闭K,点燃D处酒精灯。A中产生N2的作用是 ,C中盛装的试剂应是 。
(4)装置A中发生反应的离子方程式为 。
(5)若蓝绿色固体的组成为xCuCO3·yCu(OH)2,实验能观察到的现象是 。
(6)同学们查阅文献知:Ksp[CaCO3]=2.8×10-9,Ksp[BaCO3]=5.1×10-9,经讨论认为需要用Ba(OH)2代替Ca(OH)2来定量测定蓝绿色固体的化学式,其原因是 。
a.Ba(OH)2的碱性比Ca(OH)2强
b.Ba(OH)2溶解度大于Ca(OH)2,能充分吸收CO2
c.相同条件下,CaCO3的溶解度明显大于BaCO3
d.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
待D中反应完全后,打开活塞K,再次滴加NaNO2溶液产生N2,其目的是 。若定量分析所取蓝绿色固体质量为27.1 g,装置F中使用Ba(OH)2溶液,实验结束后,装置E的质量增加2.7 g,F中产生沉淀19.7 g。则该蓝绿色固体的化学式为 。
查看答案和解析>>
科目:高中化学 来源:2017届天津市五区县高三上学期期末考试化学试卷(解析版) 题型:选择题
根据下列实验操作和现象所得结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 用玻璃棒蘸取某溶液进行焰色反应实验,火焰呈黄色 | 溶液中含有Na+ |
B | 向浓度均为0.1 mol·L-1的FeCl3和AlCl3混合溶液中滴加NaOH溶液,出现红褐色沉淀。 | Ksp[Fe(OH)3]<Ksp[Al(OH)3] |
C | 室温下,用pH试纸测得:0.1 mol·L-1 Na2CO3溶液的pH约为11;0.1 mol·L-1 NaHCO3溶液的pH约为8。 | HCO3-结合H+的能力比CO32-的强 |
D | 用Fe3+浓度相同的FeCl3溶液和Fe2(SO4)3溶液,分别清洗做完银镜反应的试管,FeCl3溶液清洗得干净 | 存在可逆过程: Fe3++Ag |
查看答案和解析>>
科目:高中化学 来源:2017届天津市五区县高三上学期期末考试化学试卷(解析版) 题型:选择题
已知某离子反应为:8Fe2++NO3-+10H+=NH4++8Fe3++3H2O,下列说法不正确的是
A.Fe2+为还原剂,NO3-被还原
B.消耗l mol氧化剂,转移电子8 mol
C.氧化产物与还原产物的物质的量之比为1︰8
D.若把该反应设计为原电池,则负极反应式为 Fe2+-e-=Fe3+
查看答案和解析>>
科目:高中化学 来源:2017届四川省资阳市高三第二次诊断性考试化学试卷(解析版) 题型:选择题
25℃时,用0.1000 mol·L-1 KOH溶液滴定20.00 mL 0.1000 mol·L-1 CH3COOH溶液,滴定中pH变化如图,下列关系错误的是

A.V=0.00mL时,CH3COOH溶液pH=3,其电离平衡常数K≈10-5mol·L-1
B.V=10.00mL时,溶液中c(CH3COO-)>c(K+)>c(H+)>c(OH-)
C.溶液pH=7时,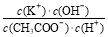 =1
=1
D.V≥20.00mL时,溶液中c(K+)=c(CH3COO—)+c(OH-)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省惠州市高二上学期高二质量检测化学试卷(解析版) 题型:实验题
硫酸铜的制备实验是无机化学实验教学中一个必做实验,某研究性学习小组设计了如下两个实验方案:
实验一:
因铜不能与稀硫酸反应,实验中用铜和浓硫酸加热使之完全反应,将溶液通过蒸发、结晶等操作得到硫酸铜晶体。
(1)浓硫酸与稀硫酸相比较,浓硫酸具有 。
(2)该反应的化学方程式为 。
实验二:
以空气为氧化剂的一步氧化法,将空气或氧气直接通入到铜粉与稀硫酸的混合物中,反应原理为2Cu + O2 + 2H2SO4 = 2CuSO4 + 2H2O ,但反应速率太慢,当升高温度到80~90℃,反应仍然缓慢。如在铜粉和稀硫酸的混合物中加入少量Fe2(SO4)3溶液,则速率明显加快。
(3)Fe2(SO4)3的作用是_________________。
(4)得到的混合液可以用下列四种物质中的_______调节pH =2~4,使Fe3+ 形成Fe(OH)3沉淀而除去:
A.NaOH B.CuO C.CuCO3 D.Fe
(5)请根据以上内容,对这两个实验方案进行评价,填下表:(至少写一点)
实 验 (一) | 实 验 (二) | |
主要优 点 | 操作简便 | (1)原料充分转化为产品 (2)没有有害气体排放 |
主要缺 点 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省惠州市高二上学期高二质量检测化学试卷(解析版) 题型:选择题
能在水溶液中大量共存的一组离子是
A.H+、I-、NO 、SiO32- B.NH4+、OH-、Cl-、HCO3-
、SiO32- B.NH4+、OH-、Cl-、HCO3-
C.K+、SO42-、Cu2+、NO3- D.Al3+、Mg2+、SO 、CO32-
、CO32-
查看答案和解析>>
科目:高中化学 来源:2016-2017黑龙江牡丹江第一高级中学高一上期末化学卷(解析版) 题型:选择题
下列关于物质检验的说法中正确的是( )
A.往某溶液中滴加BaCl2溶液,产生白色沉淀,则原溶液中一定含SO42—
B.往某溶液中通入CO2,产生白色沉淀,则原溶液中一定含SiO32—
C.取某溶液进行焰色反应,透过蓝色钴玻璃 焰色为紫色,则原溶液的溶质一定就是钾盐
焰色为紫色,则原溶液的溶质一定就是钾盐
D.往某溶液中滴加稀硝酸酸化的硝酸银溶液,产生白色沉淀,则原溶液中一定含Cl—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com