
| A��Al2��SO4��3��Һ�μӰ�ˮ������ɫ��״������Al3++3OH-�TAl��OH��3�� |
| B��90��ʱ����ô�ˮ��c��H+��?c��OH-���T3.8��10-13��H2O��l��?H+��aq��+OH-��aq����H��0 |
| C��FeCl3��Һ��ͨ��SO2����Һ��ɫ��ȥ��2Fe3++SO2+2H2O�T2Fe2++SO42-+4H+ |
| D��̼������Һ�����̪��죺CO32-+2H2O?H2CO3+2OH- |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������Һ�п϶�����I- |
| B������Һ�п��ܺ���Ba2+ |
| C������Һ�п϶�����NH4+ |
| D������Һ�п��ܺ���MnO4- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ȫ�� | B�����ܢ� |
| C�����٢ڢ� | D�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Fe2+ |
| B��Fe3+��Fe2+ |
| C��Fe3+ |
| D��Fe3+��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��7.8g Na2O2���еĹ��ۼ���Ϊ0.2NA |
| B��7.8 g Na2S��Na2O2�Ļ�������������Ϊ0.3 NA |
| C��7.8g Na2O2��������CO2��ַ�Ӧ��ת�Ƶĵ���Ϊ0.2NA |
| D��0.2 mol Na����ȫ��������7.8g Na2O2��ת�Ƶ��ӵ���ĿΪ0.4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ʹ�õIJ��Ǵ������������ǵĺϽ� |
| B��Ŀǰ���ƵõĴ�����ֻ��90���֣����ƵõĺϽ��ѴXǧ�� |
| C����������� |
| D���������ʰ�װ���˷ѽ�����������ɻ�����Ⱦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
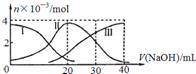 �����£���20mL 0.2mol/L H2A��Һ�еμ�0.2mol/L NaOH��Һ���й��������ʵ����仯��ͼ������˵����ȷ���ǣ�������
�����£���20mL 0.2mol/L H2A��Һ�еμ�0.2mol/L NaOH��Һ���й��������ʵ����仯��ͼ������˵����ȷ���ǣ�������| A���μӹ����е���Һ������ʱ��V��NaOH����20mL |
| B����V��NaOH��=30mLʱ�����У�2c��Na+��=3c��A2-��+3c��HA-�� |
| C��H 2A��ˮ�еĵ��뷽��ʽ�ǣ�H 2A��H++HA-�� HA-?H++A2- |
| D����V��NaOH��=20mLʱ�����У�c��Na+����c��HA-����c��H+����c��A2-����c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ᡢʳ�Ρ�ˮ�� |
| B��ˮ������������� |
| C�����ͭ�̡�Ư�� |
| D���ɱ���Һ�����ƾ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com