
| A. | +3 | B. | +1 | C. | +4 | D. | +2 |
科目:高中化学 来源: 题型:选择题
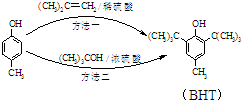 BHT是一种常用的食品抗氧化剂,从
BHT是一种常用的食品抗氧化剂,从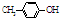 出发合成BHT的方法有如图两种.下列说法错误的是
出发合成BHT的方法有如图两种.下列说法错误的是| A. | BHT与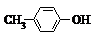 都能使酸性KMnO4褪色 都能使酸性KMnO4褪色 | |
| B. | BHT在水中的溶解度小于苯酚 | |
| C. | 两种方法的反应类型都是加成反应 | |
| D. | 从绿色化学角度分析方法一优于方法二 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①③④ | C. | ③④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
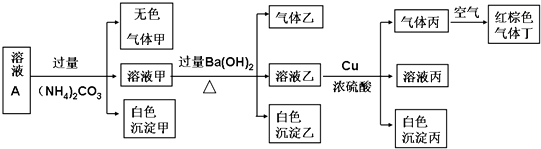
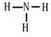
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | ①②④⑤ | C. | ①③⑤ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg和Al | B. | Al和Fe | C. | Fe和Cu | D. | Na和Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 纯碱溶液中加入苯酚:CO32-+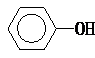 → →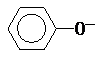 +HCO3- +HCO3- | |
| B. | 小苏打溶液中加醋酸溶液:HCO3-+CH3COOH→CO2↑+CH3COO- | |
| C. | 明矾溶液中加入过量的Ba(OH)2溶液:Al3++4OH-→AlO2-+2H2O | |
| D. | 氯化铵溶于水:NH4++2H2O?H3O++NH3•H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com