

| ||
| 1.5 |
| 11.2L-6.72L |
| 22.4L/mol |
| ||
| 1.5L |


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
| 实验步骤和方法 | 实验现象 |
| ①把7瓶液体分别依次标号A、B、C、D、E、F、G后闻气味 | 只有F、G两种液体没有气味 |
| ②各取少量于试管中加水稀释 | 只有C、D、E三种液体不溶解而浮在水上层 |
| 分别取少量7种液体于试管中加新制的Cu(OH)2并加热 | 只有B使沉淀溶解,F中产生红色沉淀 |
| 各取C、D、E少量于试管中,加稀NaOH溶液并加热 | 只有C仍有分层现象,且在D的试管中闻到特殊香味 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 组别 | 被选出的物质 | 挑选依据 |
| 第(1)组 | S | 其它三种为气体 |
| 第(2)组 | ||
| 第(3)组 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
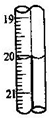 硫代硫酸钠的纯度可用滴定法进行测定,原理是:2S2O32-+I2→S4O62-+2I-
硫代硫酸钠的纯度可用滴定法进行测定,原理是:2S2O32-+I2→S4O62-+2I-| 编号 | 1 | 2 | 3 |
| 消耗I2溶液的体积/mL | 19.98 | 20.02 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原电池是把电能转为化学能的装置 |
| B、原电池中的阳离子向正极移动 |
| C、原电池两极均发生氧化还原反应 |
| D、原电池中电子流出的一极是正极,发生氧化反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com