
化学反应可视为旧键的断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol 化学键时释放(或吸收)出的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(KJ•mol﹣1)P﹣P:198 P﹣O:360 O=O:498 则反应P4(白磷)+3O2→P4O6 的反应热△H为()

A. +1638KJ•mol﹣1 B. ﹣1638KJ•mol﹣1
C. +126KJ•mol﹣1 D. ﹣126KJ•mol﹣1
考点: 有关反应热的计算.
专题: 化学反应中的能量变化.
分析: 化学反应中旧键断裂需要吸收能量,新键形成需要放出能量,化学反应中的反应热△H=反应物总键能﹣生成物总键能,据此计算出反应P4(白磷)+3O2→P4O6的反应热,注意每摩尔P4中含有6molP﹣P键.
解答: 解:各化学键键能为:P﹣P 198kJ•mol﹣1、P﹣O 360kJ•mol﹣1、O=O 498 kJ•mol﹣1,
反应热的焓变:△H=反应物总键能﹣生成物总键能,则反应P4(白磷)+3O2→P4O6的反应热为:△H=6×198kJ•mol﹣1+3×498kJ•mol﹣1﹣12×360kJ•mol﹣1=﹣1638kJ•mol﹣1,
故选B.
点评: 本题考查反应热与化学键键能的关系,题目难度中等,注意从物质能量、键能角度理解反应热,明确反应热的焓变△H=反应物总键能﹣生成物总键能及焓变的正负与吸收、放热热量的关系.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
(1)同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为 ,物质的量之比为 ,原子总数之比为 ,密度之比为 .
(2)在标准状况下,4g H2、11.2L O2、1mol H2O中,所含分子数最多的是 ,含原子数最多的是 ,体积最小的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
关于化学键的下列叙述中,正确的是( )
|
| A. | 离子化合物一定含共价键 |
|
| B. | 共价化合物可能含离子键 |
|
| C. | 离子化合物中只含离子键 |
|
| D. | 共价化合物中肯定不含离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
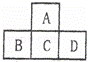
有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素的原子核外共有56个电子,在周期表中的位置如图所示.E元素的最高价氧化物既能与强酸反应又能与强碱反应.请回答:
(1)写出下列元素的元素符号:A 、B 、D .
(2)A元素与氢元素形成的H2A化合物分子中,所含化学键为 键(填“离子”或“极性”或“非极性”),用电子式表示H2A的形成过程 , .
(3)A元素与E元素形成的化合物的化学式是 ,该化合物在物质分类中属于 氧化物.(填“酸性”,“碱性”或“两性”)
(4)向D元素与E元素形成的化合物的水溶液中滴加NaOH溶液,开始时,实验现象是 有 ,反应的离子方程式为 ;继续滴加NaOH溶液至过量,实验现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
已知两个热化学方程式:C(s)+O2(g)═CO2(g)△H=﹣393.5kJ/mol2H2(g)+O2(g)═2H2O(g)△H=﹣483.6kJ/mol.现有炭粉和H2组成的悬浮气共0.3mol,使其在O2中完全燃烧,共放出87.71kJ的热量,则炭粉与H2的物质的量之比是()
A. 1:1 B. 1:2 C. 2:3 D. 3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z为三种气体.把 a molX和 b molY充入一密闭容器中.发生反应X+2Y⇌2Z 达到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转化率为()
A. [ ]×100% B. [
]×100% B. [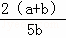 ]×100% C. [
]×100% C. [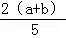 ]×100% D. [
]×100% D. [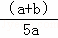 ]×100%
]×100%
查看答案和解析>>
科目:高中化学 来源: 题型:
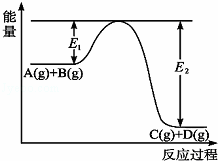
反应A(g)+B(g)⇌C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
(1)该反应是 (填“吸热”或“放热”)反应.
(2)当反应达到平衡时,升高温度,A的转化率减小(填“增大”“减小”或“不变”),原因是 .
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1 ,E2 (填“增大”“减小”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,盐酸溶液的pH是4,氯化铵溶液的pH是5,盐酸与氯化铵溶液中水电离的c(H+)之比为()
A. 10:1 B. 1:10 C. 1:105 D. 105:1
查看答案和解析>>
科目:高中化学 来源: 题型:
在相同条件下,下列三个化学反应放出的热量分别以△H1、△H2、△H3表示:
(1)2H2(g)+O2(g)═2H2O(g)△H1
(2)2H2(g)+O2(g)═2H2O(l)△H2
(3)H2(g)+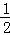 O2(g)═H2O(g)△H3
O2(g)═H2O(g)△H3
则△H1、△H2和△H3的关系是()
A. △H1=△H2=△H3 B. △H1<△H2,△H3=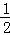 △H1
△H1
C. △H1>△H2,△H2=2△H3 D. 无法比较
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com