
| A. | 碱石灰 | B. | 正丁烷 | C. | 合金 | D. | 铝热剂 |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 元素 | 结构或性质信息 |
| X | 其原子最外层电子数是内层电子数的2倍 |
| Y | 基态原子最外层电子排布为nsnnpn+1 |
| Z | 非金属元素,其单质为固体,在氧气中燃烧时有明亮的蓝紫色火焰 |
| M | 单质在常温、常压下是气体.基态原子的M层上有1个未成对的p电子 |
| Q | 其与X形成的合金为目前用量最多的金属材料 |
 .
.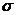 键和π键数目之比为1:1.
键和π键数目之比为1:1.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 元素 | 有关信息 |
| A | 位于第二周期第 VIA族 |
| B | 焰色反应呈黄色 |
| C | 无机非金属材料的主角 |
| D | 与A同主族 |
| E | 原子序数比D多1 |
 ,该化合物含有离子键(填“离子键”或“共价键”).
,该化合物含有离子键(填“离子键”或“共价键”).查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 硫酸工业中二氧化硫的催化氧化,不采用高压是因为压强对SO2转化率无影响 | |
| B. | 同温、同浓度的盐酸和氢氧化钠稀溶液中,水的电离程度相同 | |
| C. | 3C(s)+CaO(s)═CaC2(s)+CO(g)在常温下不能自发进行,说明该反应的△H>0 | |
| D. | 合成氨时,其他条件不变升高温度,反应速率v(H2)和氢气的平衡转化率均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热能要充分利用 | |
| B. | 燃料充分燃烧时输入的空气量越多越好 | |
| C. | 固体燃料燃烧前要粉碎 | |
| D. | 液体燃料燃烧时可以雾状喷出 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Al3+ Mg2+ Cl- NO3- | B. | Na+ Fe3+ Al3+ OH- | ||
| C. | K+ NH4+ | D. | Na+ K+ CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下.11.2LNH3中含有N一H键的数目为1.5N | |
| B. | 足量的铜与含2mo1H2SO4的浓硫酸充分反应.可生成NA个SO2分子 | |
| C. | 标准状况下.将11.2LC12通人足量的石灰乳中制备漂白粉.转移的电子数为0.5NA | |
| D. | 常温常压下.21g氧气和27g臭氧所含的氧原子总数为3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com