
【题目】治理汽车尾气和燃煤尾气是环境保护的重要课题.请回答下列问题:
(1)在汽车排气系统中安装三元催化转化器,可发生反应:2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g).在恒容密闭容器中通入等量的CO和NO,发生上述反应时,c(CO)随温度(T)和时间(t)的变化曲线如图所示.
2CO2(g)+N2(g).在恒容密闭容器中通入等量的CO和NO,发生上述反应时,c(CO)随温度(T)和时间(t)的变化曲线如图所示.
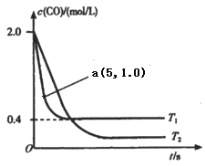
①据此判断该反应的正反应为____(填“放热”或“吸热”)反应.
②温度T1时,该反应的平衡常数K=_____;反应速率v=v(正)-v(逆)=k正c2(NO)c2(CO)- k逆c2(CO2)c(N2),k正、k逆分别为正、逆反应速率常数,计算a处v(正):v(逆)=________.
(2)下图流程是一种新型的除去尾气中氮氧化物的技术,一般采用氨气或尿素作还原剂
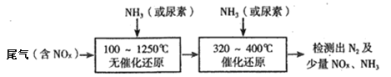
该技术中用尿素[CO(NH2)2]作还原剂还原NO2的主要反应为:4CO(NH2)2+6NO2![]() 4CO2+7N2+8H2O ,则用NH3作还原剂还原尾气中NO(NH3、NO的物质的量之比为1:1)的化学方程式为:______.
4CO2+7N2+8H2O ,则用NH3作还原剂还原尾气中NO(NH3、NO的物质的量之比为1:1)的化学方程式为:______.
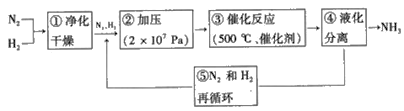
(3)哈伯法合成氨的流程图如图,下列五个流程中为提高原料利用率而采取的措施________(填序号)
(4)一种电化学制备NH3的装置如图所示,图中陶瓷在高温时可以传输H+.下列叙述正确的是______________(填选项)
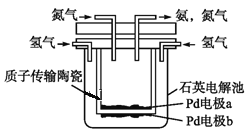
A.Pd电极b为阴极 B.阴极的反应式为N2+6H++6e-=2NH3
C.H+由阳极向阴极迁移 D.陶瓷可以隔离N2和H2
(5)也可用CH4催化还原NOx法消除烟气中氮氧化物的污染.已知:
①CH4(g)+ 2NO2(g)= N2(g)+CO2(g)+2H2O(g) △H=-867.0kJ/mol;
②N2(g)+2O2(g)= 2NO2(g) △H=+67.0 kJ/mol;
③N2(g)+O2(g)=2NO(g) △H=+89.0 kJ/mol
则CH4催化还原NO的热化学方程式为__________________________________.
【答案】放热 80 160:1 4NH3+4NO+O2(g)=4N2+6H2O ②④⑤ BCD CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H =-978.0 kJ/mol
【解析】
(1)①从图中可以看出,T1时反应先达平衡,则T1>T2,T1时c(CO)大,说明升高温度,平衡逆向移动。
② 依题意,可得如下三段式:

温度T1时,该反应的平衡常数K=![]() ,反应速率v=v(正)-v(逆)=k正c2(NO)c2(CO)- k逆c2(CO2)c(N2),k正、k逆分别为正、逆反应速率常数,平衡时,k正c2(NO)c2(CO)=k逆c2(CO2)c(N2),即k正×0.42×0.42=k逆×0.8×1.62,k正=80 k逆。
,反应速率v=v(正)-v(逆)=k正c2(NO)c2(CO)- k逆c2(CO2)c(N2),k正、k逆分别为正、逆反应速率常数,平衡时,k正c2(NO)c2(CO)=k逆c2(CO2)c(N2),即k正×0.42×0.42=k逆×0.8×1.62,k正=80 k逆。

计算a处v(正):v(逆)= k正c2(NO)c2(CO:k逆c2(CO2)c(N2)= 80 k逆×1.02×1.02: k逆×0.5×1.02=160:1
(2)用NH3作还原剂还原尾气中NO(NH3、NO的物质的量之比为1:1),NO得2e-,NH3失去3e-,得失电子总数不等,则另有得电子的物质,只能为空气中的O2,由此可得出反应的化学方程式。
(3)五个流程中为提高原料利用率而采取的措施:加压,有利于平衡正向移动,提高反应物的转化率;加催化剂只能加快反应速率,但不能使平衡发生移动;液化分离NH3,虽然不能加快反应速率,但能使平衡正向移动;N2和H2循环使用,也可提高反应物的转化率。
(4)从图中可以看出,H2失电子,Pd电极b为阳极,则Pd电极a为阴极。
A.Pd电极b为阳极,A错误;
B.阴极N2得电子,生成NH3,电极反应式为N2+6H++6e-=2NH3,B正确;
C.阳极生成H+,通过质子传输陶瓷向阴极迁移,C正确;
D.陶瓷只允许H+通过,可以隔离N2和H2,D正确。
(5) ①CH4(g)+ 2NO2(g)= N2(g)+CO2(g)+2H2O(g) △H=-867.0kJ/mol;
②N2(g)+2O2(g)= 2NO2(g) △H=+67.0 kJ/mol;
③N2(g)+O2(g)=2NO(g) △H=+89.0 kJ/mol
则①+②-③×2可得CH4催化还原NO的热化学方程式。
(1)①从图中可以看出,T1时反应先达平衡,则T1>T2,T1时c(CO)大,说明升高温度,平衡逆向移动,从而得出正反应为放热反应。答案为:放热;
② 依题意,可得如下三段式:

温度T1时,该反应的平衡常数K=![]() =80,反应速率v=v(正)-v(逆)=k正c2(NO)c2(CO)- k逆c2(CO2)c(N2),k正、k逆分别为正、逆反应速率常数,平衡时,k正c2(NO)c2(CO)=k逆c2(CO2)c(N2),即k正×0.42×0.42=k逆×0.8×1.62,k正=80 k逆。
=80,反应速率v=v(正)-v(逆)=k正c2(NO)c2(CO)- k逆c2(CO2)c(N2),k正、k逆分别为正、逆反应速率常数,平衡时,k正c2(NO)c2(CO)=k逆c2(CO2)c(N2),即k正×0.42×0.42=k逆×0.8×1.62,k正=80 k逆。

计算a处v(正)v(逆)= k正c2(NO)c2(CO:k逆c2(CO2)c(N2)= 80 k逆×1.02×1.02: k逆×0.5×1.02=160:1。答案为:80;160:1;
(2)用NH3作还原剂还原尾气中NO(NH3、NO的物质的量之比为1:1),NO得2e-,NH3失去3e-,得失电子总数不等,则另有得电子的物质,只能为空气中的O2,由此可得出反应的化学方程式4NH3+4NO+O2(g)=4N2+6H2O。答案为:4NH3+4NO+O2(g)=4N2+6H2O;
(3)五个流程中为提高原料利用率而采取的措施:加压,有利于平衡正向移动,提高反应物的转化率;加催化剂只能加快反应速率,但不能使平衡发生移动;液化分离NH3,虽然不能加快反应速率,但能使平衡正向移动;N2和H2循环使用,也可提高反应物的转化率。答案为:②④⑤;
(4)从图中可以看出,H2失电子,Pd电极b为阳极,则Pd电极a为阴极。
A.Pd电极b为阳极,A错误;
B.阴极N2得电子,生成NH3,电极反应式为N2+6H++6e-=2NH3,B正确;
C.阳极生成H+,通过质子传输陶瓷向阴极迁移,C正确;
D.陶瓷只允许H+通过,可以隔离N2和H2,D正确。答案为:BCD;
(5) ①CH4(g)+ 2NO2(g)= N2(g)+CO2(g)+2H2O(g) △H=-867.0kJ/mol;
②N2(g)+2O2(g)= 2NO2(g) △H=+67.0 kJ/mol;
③N2(g)+O2(g)=2NO(g) △H=+89.0 kJ/mol
则①+②-③×2可得CH4催化还原NO的热化学方程式为CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H =-978.0 kJ/mol。答案为:CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H =-978.0 kJ/mol。


 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:
【题目】某化学学习小组欲探究己烷的性质,用己烷进行下列实验:
实验1:

实验2:将上述橙色溶液装入密封性好的无色试剂瓶中。过一段时间,溶液颜色变浅,打开瓶盖瓶口出现白雾。
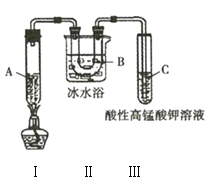
实验3:利用如图所示实验装置在一定条件分解己烷(生成丙烷和丙烯![]() ),且丙烯能被酸性
),且丙烯能被酸性![]() 溶液氧化。
溶液氧化。
(1)实验1中用到的玻璃仪器主要有______________________________________(填名称)。
(2)由实验1可知,己烷的物理性质有____________________________________。
(3)实验2中的橙色溶液逐渐变浅的原因是__________________(填序号)。
A.己烷与溴发生了取代反应
B.溴代己烷为无色物质
C.液溴向外挥发浓度降低
D.己烷与液溴发生了加成反应
E.液溴与己烷分层,密度大的液溴在下层
(4)实验3中装置Ⅱ的作用是______________________________________。
(5)试管C中的现象是______________________________________。
(6)试写出装置Ⅰ中发生的生成丙烷和丙烯的化学方程式:______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜的化合物如Cu2O、CuO、CuCl、CuSO4·5H2O、Cu(IO3)2、[Cu(H2NCH2CH2NH2)2]Cl2等均有着广泛的应用.回答下列问题:
(1)基态Cu2+的核外电子排布式为____________
(2)IO3-的空间构型为_____________________________(用文字描述),与SO42-互为等电子体的分子为____________
(3)配离子[Cu(H2NCH2CH2NH2)2]2+中,Cu2+的配位数是____________.
①乙二胺分子中N 原子轨道的杂化类型为____________.
② 1mol [Cu(H2NCH2CH2NH2)2]2+ 中含有的σ键的数目为____________.
(4)CuO的熔点比CuCl的熔点高,其原因是____________.
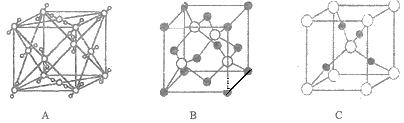
(5)Cu2O晶体结构可能是____________ (填字母).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示装置中,观察到电流计指针偏转,M棒变粗,N棒变细,其中P为电解质溶液。由此判断M、N、P所代表的物质可能是( )
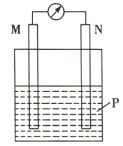
选项 | M | N | P |
A | 锌 | 铜 | 稀硫酸 |
B | 铜 | 锌 | 稀硫酸 |
C | 银 | 锌 | AgNO3溶液 |
D | 铜 | 铁 |
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应I2(g)+H2(g) ![]() 2HI(g) ΔH<0,下列说法正确的是( )
2HI(g) ΔH<0,下列说法正确的是( )
A.降低温度,正向反应速率减小倍数大于逆向反应速率减小倍数
B.升高温度将缩短达到平衡的时间
C.达到平衡后,保持温度和容积不变,充入氩气,正、逆反应速率同等倍数增大
D.达到平衡后,保持温度和压强不变,充入氩气,HI的质量将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A.向NaOH溶液中通入过量CO2:2OH-+CO2=CO32-+H2O
B.电解氯化镁溶液:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C.向H2O2溶液中加入MnO2:2H2O2+4H++MnO2=O2↑+Mn2++4H2O
D.向KAl(SO4)2溶液中滴加Ba(OH)2溶液至SO42—沉淀完全:Al3++2SO42—+2Ba2++4OH—=AlO2-+2BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化镓(GaN)被称为第三代半导体材料,其应用已经取得了突破性的进展。
已知:(i)氮化镓性质稳定,不与水、酸反应,只在加热时溶于浓碱。
(ii)NiCl2 溶液在加热时,先转化为Ni(OH)2,后分解为NiO。
(iii)制备氮化镓的反应为:2Ga+2NH3![]() 2GaN+3H2
2GaN+3H2
某学校化学兴趣小组实验室制备氮化镓,设计实验装置如图所示:
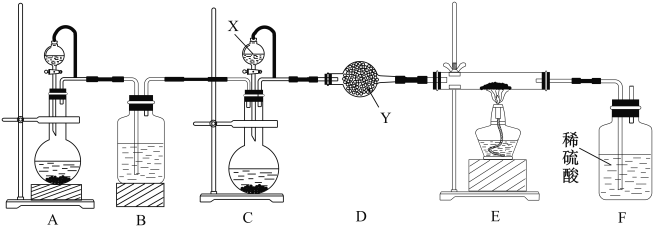
设计实验步骤如下:
①滴加几滴NiCl2 溶液润湿金属镓粉末,置于反应器内。
②先通入一段时间后的H2,再加热。
③停止通氢气,改通入氨气,继续加热一段时间。
④停止加热,继续通入氨气,直至冷却。
⑤将反应器内的固体转移到盛有盐酸的烧杯中,充分反应过滤、洗涤、干燥。
(1)仪器X中的试剂是___________,仪器Y的名称是__________________。
(2)指出该套装置中存在一处明显的错误是________________________。
(3)步骤①中选择NiCl2 溶液,不选择氧化镍的原因是____________________。
a.增大接触面积,加快化学反应速率
b使镍能均匀附着在镓粉的表面,提高催化效率
c.为了能更好形成原电池,加快反应速率
(4)步骤③中制备氮化镓,则判断该反应接近完成时观察到的现象是____________________。
(5)请写出步骤⑤中检验产品氮化镓固体洗涤干净的操作________________________。
(6)镓元素与铝同族,其性质与铝类似,请写出氮化镓溶于热NaOH溶液的离子方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向体积恒定为2L的密闭容器里充入2mol M和一定量的N,发生如下反应:M(g)+N(g)![]() E(g),当反应进行到4min时达到平衡,测得M的浓度为0.2mol·L-1。下列说法正确的是( )
E(g),当反应进行到4min时达到平衡,测得M的浓度为0.2mol·L-1。下列说法正确的是( )
A.2min时,M的物质的量浓度为0.6mol·L-1
B.0~4min内,v(M)=0.8mol·L-1·min-1
C.4min后,向容器中充入不参与反应的稀有气体,M的物质的量减小
D.4min时,M的转化率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中,可逆反应:A2(g)+ B2(g)![]() xC(g) 符合下列图Ⅰ所示关系,由此推断对图Ⅱ的正确说法是
xC(g) 符合下列图Ⅰ所示关系,由此推断对图Ⅱ的正确说法是
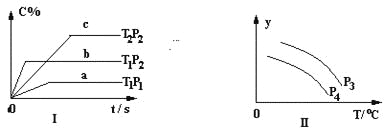
A. P3<P4,Y轴表示A2的转化率
B. P3<P4,Y轴表示A2的浓度
C. P3>P4,Y轴表示混合气体的密度
D. P3>P4,Y轴表示混合气体的平均摩尔质量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com