
| A. | 2个-CH3,能生成4种一氯代物 | B. | 3个-CH3,能生成4种一氯代物 | ||
| C. | 3个-CH3,能生成5种一氯代物 | D. | 4个-CH3,能生成4种一氯代物 |
分析 分子式为C6H14的有机物属于烷烃,含有6个C原子,为己烷,先根据甲基数目写出符合条件的同分异构体的结构简式,然后利用等效氢判断其一氯代物的数目即可.
解答 解:A.己烷分子中含2个甲基,其结构简式为:CH3CH2CH2CH2CH2CH3,分子中含有3种H原子,则有3种一氯代物,故A错误;
B.己烷分子中含3个甲基,其结构简式为: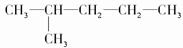 、
、 ,前者含有5种一氯代物,后者含有4种一氯代物,故B正确;
,前者含有5种一氯代物,后者含有4种一氯代物,故B正确;
C.己烷分子中含有含3个甲基的结构简式为: 、
、 ,前者含有5种一氯代物,后者含有4种一氯代物,故C正确;
,前者含有5种一氯代物,后者含有4种一氯代物,故C正确;
D.己烷分子中含有4个甲基的结构简式为: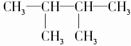 、
、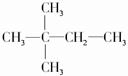 ,前一种有2种一氯代物,后一种有3种一氯代物,故D错误;
,前一种有2种一氯代物,后一种有3种一氯代物,故D错误;
故选BC.
点评 本题考查同分异构体的书写及判断,题目难度不大,根据甲基数目书写符合条件的同分异构体结构是关键,注意掌握同分异构体的概念及书写原则,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:解答题
 (1)CO2分子的电子式为
(1)CO2分子的电子式为 ;Na2O2的电子式为
;Na2O2的电子式为
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 (25°C)) | Ki=1.77×10-14 | Ki=4.9×10-14 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温pH=3的硫酸与pH=11的LiOH溶液等体积混合溶液呈碱性,说明LiOH为强碱 | |
| B. | 用明矾净水是因为Al3+水解生成的Al(OH)3胶粒能凝聚水中的悬浮物 | |
| C. | 除去MgCl2溶液中的FeCl3,可向其中加入MgCO3 | |
| D. | 除去锅炉水垢中的CaSO4,可加入Na2CO3溶液将其转化为CaCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 t℃时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.
t℃时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.| t/min | X/mol | Y/mol | Z/mol |
| 0 | 2.00 | 4.00 | 0 |
| 1 | 1.80 | 3.60 | 0.40 |
| 3 | 1.65 | 3.30 | 0.70 |
| 5 | 1.55 | 3.10 | 0.90 |
| 14 | 1.00 | 2.00 | 2.00 |
| 16 | 1.00 | 2.00 | 2.00 |
| 20 | 0.50 | 4.24 | 3.00 |
| 22 | 0.50 | 4.24 | 3.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
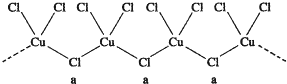 铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制造、国防等领域.一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO).
铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制造、国防等领域.一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO). 杂化轨道类型sp2
杂化轨道类型sp2 杂化轨道类型sp3.
杂化轨道类型sp3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 如果盐酸的浓度是醋酸的两倍,则盐酸中的H+浓度也是醋酸中的两倍 | |
| B. | 将NaOH溶液和氨水各稀释一份,两者的OH-浓度均减小到原来的$\frac{1}{2}$ | |
| C. | 中和等体积、等物质的量浓度的盐酸和醋酸溶液,盐酸所需氢氧化钠多于醋酸 | |
| D. | 若电解质溶液的导电能力也可能比强电解质溶液的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2+O2$\frac{\underline{\;高温\;}}{\;}$2H2O | B. | CaO+CO2═CaCO3 | ||
| C. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | D. | C2H5OH+3O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol铁在0.1mol氯气中燃烧,电子转移0.2NA个 | |
| B. | 标准状况下,2.24 L Cl2溶于水所得溶液中含有Cl_0.2 NA | |
| C. | 1.12 L氧气中含有0.1 NA个氧原子 | |
| D. | 1mol二氧化碳和足量的过氧化钠反应时转移电子数为2NA个 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com