
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:解答题

 .D物质的名称是乙醛.
.D物质的名称是乙醛.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 有机物A属于醛类 | B. | 有机物A与B属于同系物 | ||
| C. | 有机物C能与H2发生加成反应 | D. | 有机物D的一氯代物有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 K3[Fe(C2O4)3]•3H2O[三草酸合铁(Ⅲ)酸钾晶体]易溶于水,难溶于乙醇,可作为有机反应的催化剂.实验室可用废铁屑等物质为原料制备,并测定产品的纯度.相关反应的化学方程式为:
K3[Fe(C2O4)3]•3H2O[三草酸合铁(Ⅲ)酸钾晶体]易溶于水,难溶于乙醇,可作为有机反应的催化剂.实验室可用废铁屑等物质为原料制备,并测定产品的纯度.相关反应的化学方程式为:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,无水HF的作用是反应物和溶剂
,无水HF的作用是反应物和溶剂查看答案和解析>>
科目:高中化学 来源: 题型:解答题
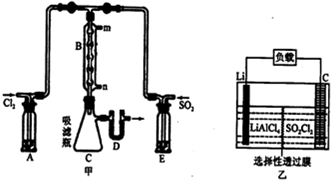
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量H2S通入NaOH溶液中;足量H2S通入NaOH溶液中 | |
| B. | 少量铁粉与硫粉共热;足量铁粉与硫粉共热 | |
| C. | 常温下Na与O2反应;Na在O2中点燃 | |
| D. | 铜与稀硝酸反应;铜与浓硝酸反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com