
| A、原混合气体中O2和CH4的体积比为2:1 |
| B、原混合气体中O2和CH4的体积比为1:2 |
| C、残留固体中有Na2CO3和Na2O2、NaOH |
| D、残留固体中只有Na2CO3 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、Br2+2NaI=I2+2NaBr |
| B、Zn+H2SO4(稀)=ZnSO4+H2↑ |
| C、2C+SiO2═Si+2CO↑ |
| D、2Al+Fe2O3═2Fe+Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、途径Ⅰ与途径Ⅱ所得混合气体的百分组成相同 |
| B、途径Ⅰ的反应速率v(N2)与途径Ⅱ的反应速率v(NH3)的比值为1:2 |
| C、途径Ⅰ平衡时NH3的浓度与途径Ⅱ平衡时NH3的浓度之比为1:2 |
| D、途径Ⅰ与途径Ⅱ所得混合气体的物质的量的之比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将pH均为a的氢氧化钠溶液和氨水分别加水稀释100倍,pH变为b和c,则a、b、c的大小关系是:a>c>b |
| B、常温下,浓度均为0.1mol/L①醋酸、②盐酸、③醋酸钠溶液,水电离程度的顺序为:③>①>② |
| C、常温下,将相同体积的pH=3硫酸和pH=11一元碱BOH溶液混合,所得溶液可能为中性也可能为酸性 |
| D、物质的浓度相同的①氯化铵溶液、②硫酸铵溶液、③碳酸氢铵溶液,pH的顺序为:③>①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:
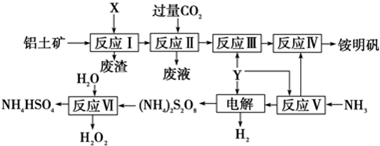
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、淀粉与稀H2SO4共热,再加银氨溶液水浴加热,无银镜生成,说明淀粉水解产物无还原性 | ||
B、SiO2+2C
| ||
| C、向NaAlO2溶液中滴加饱和NaHCO3溶液,有白色沉淀产生,是因为两者都发生了水解反应,且相互促进 | ||
| D、将CO2通入Na2SiO3溶液中,有白色沉淀生成,证明H2CO3酸性比H2SiO3强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除去CO中少量的O2,将气体反复通过灼热的Cu网后收集气体 |
| B、除去CuCl2溶液中的少量FeCl3:加入足量铜粉,充分反应后,过滤 |
| C、除去CO2中的少量SO2:通过酸性高锰酸钾溶液洗气 |
| D、除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| W | X | |
| Y | Z |
| A、X、Y、Z中最简单氢化物稳定性最弱的是Y |
| B、Z元素氧化物对应水化物的酸性一定强于Y |
| C、X元素形成的单核阴离子还原性强于Y |
| D、Z元素单质在化学反应中只表现氧化性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com