
【题目】现代高科技领域使用的新型陶瓷材料氮化硼(BN),用天然硼砂(Na2B4O710H2O)经过下列过程可以制得。
天然硼砂![]() 硼酸(H3BO3)
硼酸(H3BO3)![]() B2O3
B2O3![]() BN
BN
(1)天然硼砂所含的元素中属于同一周期且原子半径是(用元素符号填写)___>___,由天然硼砂中的三种元素形成的某种离子化合物的电子式为______。
(2)与硼元素性质最相似的元素的原子的最外层电子排布为_______,该原子核外充有电子的轨道共有____个。
(3)试写出天然硼砂与硫酸反应的化学方程式_______,制得的氮化硼有不同的结构,其中超硬、耐磨、耐高温的一种属于____晶体。制取氮化硼的反应必须在密闭的耐高温容器中进行:B2O3(s)+2NH3(g)![]() 2BN(s)+3H2O(g)+Q(Q<0)
2BN(s)+3H2O(g)+Q(Q<0)
(4)若反应在5L的密闭容器中进行,经2分钟反应炉内固体的质量减少60.0g,则用氨气来表示该反应在2分钟内的平均速率为_____,达到平衡后,增大反应容器体积,在平衡移动过程中,逆反应速率的变化状况为______。
(5)为提高生产效率,使反应速率加快的同时,化学平衡向多出产品的方向移动,可以采取的措施有_________,生产中对尾气的处理方法正确的是(填序号)_____。
A.直接排出参与大气循环 B.冷却分离所得气体可以循环使用
C.全部用来进行循环使用 D.冷却分离所得液体可作化工原料
【答案】B O ![]() 3s23p2 8 Na2B4O710H2O+H2SO4→Na2SO4+4H3BO3+5H2O 原子 0.6mol/(L·min) 先减小后增大 升高温度、通入氨气 BD
3s23p2 8 Na2B4O710H2O+H2SO4→Na2SO4+4H3BO3+5H2O 原子 0.6mol/(L·min) 先减小后增大 升高温度、通入氨气 BD
【解析】
(1)Na、B、O、H四种元素中属于同一周期的是B、O,原子半径:B>O;Na、O、H三种元素可形成离子化合物NaOH;
(2)与硼元素性质最相似的元素为硅;
(3)Na2B4O710H2O与硫酸反应得到硼酸,根据原子守恒,写出化学方程式;根据晶体具有超硬、耐磨、耐高温的性质,氮化硼属于原子晶体;
(4)根据![]() =
=![]() 计算反应速率;根据浓度对化学反应速率的影响分析逆反应速率的变化;
计算反应速率;根据浓度对化学反应速率的影响分析逆反应速率的变化;
(5)根据B2O3(s)+2NH3(g)![]() 2BN(s)+3H2O(g)+Q(Q<0),正反应为吸热反应,升高温度、通入氨气平衡向正反应方向移动;根据尾气中含有NH3和水蒸气,分析尾气处理方法。
2BN(s)+3H2O(g)+Q(Q<0),正反应为吸热反应,升高温度、通入氨气平衡向正反应方向移动;根据尾气中含有NH3和水蒸气,分析尾气处理方法。
(1)天然硼砂(Na2B4O710H2O)含有Na、B、O、H四种元素,其中Na位于第三周期,B、O位于第二周期,H位于第一周期,属于同一周期的是B、O,原子半径:B>O,Na、O、H三种元素可形成离子化合物NaOH,其电子式为![]() ,故答案为:B;O;
,故答案为:B;O;![]() ;
;
(2)硼元素位于元素周期表第二周期第ⅢA族,根据对角线规则,与硼元素性质最相似的元素为第三周期第ⅣA族的硅元素,Si原子的最外层电子排布为3s23p2,该原子核外电子排布式为1s22s2p63s23p2,因此该原子核外充有电子的轨道共有共有8个。故答案为:3s23p2;8;
(3)Na2B4O710H2O与硫酸反应得到硼酸,根据原子守恒,化学方程式为Na2B4O710H2O+H2SO4→Na2SO4+4H3BO3+5H2O;原子晶体具有超硬、耐磨、耐高温的性质,故氮化硼属于原子晶体。故答案为:Na2B4O710H2O+H2SO4→Na2SO4+4H3BO3+5H2O;原子;
(4)根据质量守恒定律,固体质量减少等于气体质量的增加,设反应的NH3的质量为x,
B2O3(s)+2NH3(g)![]() 2BN(s)+3H2O(g), 质量差
2BN(s)+3H2O(g), 质量差
2×17 3×18 20
x 60.0g
![]() =
=![]() ,x=102g,
,x=102g,
则用氨气来表示该反应在2分钟内的平均速率为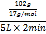 =0.6mol/(L·min);达到平衡后,增大反应容器体积,H2O(g)的浓度减小,逆反应速率减小,由于减小压强平衡正向移动,随着反应进行,H2O(g)的浓度又逐渐增大,所以逆反应速率先减小后增大;故答案为:0.6mol/(L·min);先减小后增大;
=0.6mol/(L·min);达到平衡后,增大反应容器体积,H2O(g)的浓度减小,逆反应速率减小,由于减小压强平衡正向移动,随着反应进行,H2O(g)的浓度又逐渐增大,所以逆反应速率先减小后增大;故答案为:0.6mol/(L·min);先减小后增大;
(5)根据B2O3(s)+2NH3(g)![]() 2BN(s)+3H2O(g)+Q(Q<0),正反应为吸热反应,升高温度、通入氨气使反应速率加快的同时,化学平衡向多出产品的方向移动;由反应过程可知,尾气中含有未反应的NH3和生成的水蒸气,则
2BN(s)+3H2O(g)+Q(Q<0),正反应为吸热反应,升高温度、通入氨气使反应速率加快的同时,化学平衡向多出产品的方向移动;由反应过程可知,尾气中含有未反应的NH3和生成的水蒸气,则
A.NH3直接排出参与大气循环会污染空气,故A错误;
B.冷却分离所得NH3可以循环使用,有利于原料充分利用和环境保护,故B正确;
C.由反应B2O3(s)+2NH3(g)![]() 2BN(s)+3H2O(g)可知,生成的水蒸气不用来进行循环使用,故C错误;
2BN(s)+3H2O(g)可知,生成的水蒸气不用来进行循环使用,故C错误;
D.尾气中含有NH3和水蒸气,冷却分离后得到氨水,可作化工原料,故D正确。
综合上述分析,BD正确。故答案为:升高温度、通入氨气;BD。


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
【题目】乙炔在不同条件下可以转化成许多化合物,如图,下列叙述错误的是( )
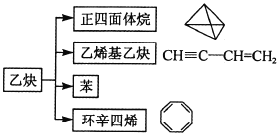
A. 正四面体烷的一氯代物及二氯代物均只有1种
B. 乙炔生成乙烯基乙炔是加成反应
C. ![]() 与环辛四烯(C8H8)互为同分异构体
与环辛四烯(C8H8)互为同分异构体
D. 等质量的苯与乙烯基乙炔完全燃烧时的耗氧量不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请完成用四氯化碳制取碘水中的碘的相关实验内容(装置图见图 2)

图 2
(1)实验步骤:装液、振荡、静置和分层、_____。
(2)实验原理:利用碘在四氯化碳中的溶解度比在水中的溶解度_____;四氯化碳与水_____;
(3)实验现象:碘的四氯化碳溶液呈_____色;碘的四氯化碳溶液在_____层;
(4)注意事项:振荡时,须不断放气,以减小分液漏斗内压强。分液时,须将分液漏斗上的玻璃塞_____________,或使玻璃塞上的凹槽(或小孔)对准漏斗上的小孔;分液时,碘的四氯化碳溶液从分液漏斗_________口倒出,水从分液漏斗 _________口流出;漏斗颈的下端要紧贴烧杯的内壁。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列反应:
①2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
②CaO+H2O=Ca(OH)2
③Ba(OH)2+H2SO4=BaSO4↓+2H2O
④Zn+2HCl=ZnCl2+H2↑
⑤2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
⑥CaCO3![]() CaO+CO2↑
CaO+CO2↑
⑦2CO+O2![]() 2CO2
2CO2
⑧SO42-+Ba2+=BaSO4↓
(1)既是分解反应又是氧化还原反应的是_____,既是化合反应又是氧化还原反应的是______(均填序号)。
(2)请用单向桥表示反应①的电子转移的方向和数目:________________。其中,该反应的氧化产物是___________,还原产物是__________。
(3)反应③的离子反应方程式为_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化剂H2O2在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注。
Ⅰ. 某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照下表所示的方案完成实验。
实验编号 | 反应物 | 催化剂 |
① | 10 mL 2% H2O2溶液 | 无 |
② | 10 mL 5% H2O2溶液 | 无 |
③ | 10 mL 5% H2O2溶液+1 mL H2O | 1 mL 0.1 mol·L-1FeCl3溶液 |
④ | 10 mL 5% H2O2溶液+1 mL HCl溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
⑤ | 10 mL 5% H2O2溶液+1 mL NaOH溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
(1)实验①和②的目的是___。同学们进行实验时没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进方法是__________(写出一种即可)。
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化如图1所示。分析该图能够得出的实验结论是____。
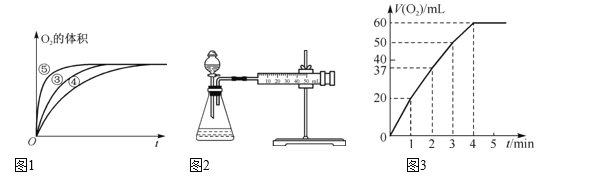
Ⅱ. MnO2对H2O2的分解有催化作用,某实验小组对H2O2的分解做了如下探究。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将状态不同的0.1 g MnO2分别加入盛有50 mL等浓度的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
MnO2状态 | 触摸试管情况 | 观察结果 | 反应完成所需时间 |
粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 4 min |
块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30 min |
(1)写出大试管中发生反应的化学方程式:__,该反应是____反应(填“放热”或“吸热”)。
(2)实验结果表明,催化剂的催化效果与____有关。
(3)实验过程中放出气体的体积(标准状况)和时间的关系如图3所示。解释反应速率变化的原因:__,计算H2O2的初始物质的量浓度为____。(保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列关于充电电池、干电池的叙述合理的是___。
①干电池可以实现化学能向电能的转化和电能向化学能的转化
②锌锰干电池长时间连续使用时内装糊状物可能流出腐蚀电器
③充电电池可以无限制地反复放电、充电
④充电是使放电时的氧化还原反应逆向进行
(2)铅蓄电池中,正极材料为PbO2,负极材料为Pb,放电时其负极反应式为___。
(3)原电池在NaOH溶液介质中,铝为负极,其负极反应式为__。
(4)航天技术中使用的氢氧燃料电池具有高能、轻便和无污染等优点。氢氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式都为2H2+O2=2H2O。
①酸式氢氧燃料电池的电解质溶液是稀硫酸,其负极反应式为2H2-4e-=4H+,则其正极反应式为____。
②碱式氢氧燃料电池的电解质溶液是KOH溶液,则其负极反应式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知(CN)2的氧化性比Br2弱而比I2强,NaCN的水溶液呈碱性,则下列有关变化一般不能发生的是
A. CH2=CH2+(CN)2→NC-CH2-CH2-CN
B. (CN)2+2Br-→2CN-+Br2
C. (CN)2+2OH-→CN-+CNO-+H2O
D. HCN![]() H++CN-
H++CN-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常见元素及化合物的转化关系如图所示:
![]()
又知A~E中均含有一种相同元素。下列说法错误的是( )
A.物质A一定是单质B.物质C可能是淡黄色固体
C.物质D可能是酸或碱D.物质E可能属于盐类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置进行的相应实验,能达到实验目的的是
A.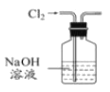 除去Cl2中含有的少量HCl
除去Cl2中含有的少量HCl
B.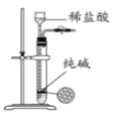 制取少量纯净的CO2气体
制取少量纯净的CO2气体
C.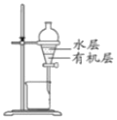 分离CC14萃取碘水后已分层的有机层和水层
分离CC14萃取碘水后已分层的有机层和水层
D.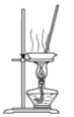 蒸干FeCl3饱和溶液制备FeCl3晶体
蒸干FeCl3饱和溶液制备FeCl3晶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com