
| A | B | C | D |
c(NaOH)/mol·L-1 | 1.0 | 0.5 | 1.0 | 0.9 |
W的成分 | Na2CO3 | Na2CO3 NaHCO3 | NaHCO3 NaOH | Na2CO3 NaHCO3 |
D
解析:n(CO2)=0.05 mol,根据碳元素守恒,若全部生成Na2CO32+,则m(Na2CO3)=106 g·mol-1×0.05 mol=5.3 g;若全部生成NaHCO3则m(NaHCO3)=84 g·mol-1×0.05 mol=4.2 g。而4.2<5.08<5.3,故为Na2CO3与NaHCO3的混合物,设Na2CO3的物质的量为x mol,则NaHCO3的物质的量为(0.05 mol-x),故106 g·mol-1·x+84 g·mol-1·(0.05 mol-x)=5.08 g,故x=0.04 mol,根据Na元素守恒n(Na+)=0.04 mol×2+(0.05-0.04) mol=0.09 mol,故c(NaOH)=![]() =0.9 mol·L-1。
=0.9 mol·L-1。


科目:高中化学 来源:陕西省师大附中2012届高三上学期期中考试化学试题 题型:058
为探究铁与浓硫酸在加热条件下的反应,某活动小组设计并完成以下实验:
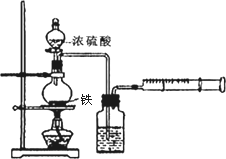
(1)实验目的:分析铁与浓硫酸在加热条件下的反应.
①洗气瓶中浓硫酸的作用是________.
②写出加热条件下铁与浓硫酸反应生成SO2的化学方程式________.
活动小组预测随着反应的进行,硫酸的浓度降低,可能还会有氢气产生,为进一步确认气体的成分还需要进行进一步的实验.
(2)实验目的:检验气体的成分.
试剂:氢氧化钠溶液、浓硫酸、氧化铜粉末、无水硫酸铜固体、品红溶液、高锰酸钾酸性溶液、碱石灰.
仪器如下图(可重复使用,可根据需要取用);
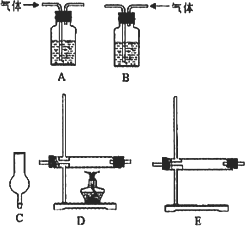
①连接仪器.将装置的字母填入□内,并将试剂名称填写在相应的括号内(可不填满)
②若混合气体中含有氢气,实验过程中能观察到的现象是________.
(3)实验目的:确定产物的含量.
①若混合气体中含有SO2和H2,为测定混合气体中各成分含量,需收集的数据有________.
②若反应后烧瓶中溶液含有的金属阳离子有Fe2+、Fe3+,其中检验是否含有Fe2+可采用的试剂为________;如果该过程中共消耗了11.2 g铁,反应后的溶液能吸收标准状况下1.12 L氯气,则原溶液中含有Fe3+的物质的量为________mol.
查看答案和解析>>
科目:高中化学 来源:2013-2014学年辽宁省新民市高三上学期期末考试化学试卷(解析版) 题型:选择题
下列有关离子方程式书写错误的是:
A.将标准状况下1.12 L氯气通入10 mL 1 mol / L的溴化亚铁溶液中:2Fe2++4Br-+3Cl2 =2Fe3++6Cl-+2Br2
B.向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液:Ca2++ HCO3- +OH- =CaCO3↓+H2O
C.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:Ba2++2OH-+H++ SO42- + NH4+=BaSO4↓+ NH3·H2O +H2O
D.向NaHSO3溶液中滴入适量NaClO溶液:HSO3– + ClO–=SO42– + H+ + Cl–
查看答案和解析>>
科目:高中化学 来源:2010年湖北襄樊四校高三上学期期中联考化学卷 题型:选择题
下列化学反应的离子方程式正确的是 ( )
A.苯酚钠溶液与少量的CO2反应: C6H5O-+CO2+H2O → C6H5OH+CO32 -
B.将标准状况下1.12 L氯气通入10 mL 1 mol / L的溴化亚铁溶液中:
2Fe2++4Br-+3Cl2 =2Fe3++6Cl-+2Br2
C.向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液:Ca2++ HCO3- +OH- =CaCO3↓+H2O
D.NH4HSO4溶液中加入足量Ba(OH)2溶液: H++SO42-+Ba2++OH-===BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
(11分) 向100mL某二价金属M的氢氧化物澄清溶液中加入过量的NaHCO3溶液后生成了MCO3沉淀。过滤,将沉淀置于足量的盐酸中,收集到标准状况下4.48L的气体;将滤液加水稀释到250 mL,取出25 mL恰好与20 mL盐酸完全反应,收集到标准状况下1.12 L的气体。请回答:
(1)M(OH)2与过量NaHCO3溶液反应的化学方程式为:
(2)要计算M的相对原子质量,你认为还必须提供下列哪项数据 (选填字母序号).
A.M的氢氧化物溶液的物质的量浓度(设为2mol/L)
B.M的碳酸盐的质量(设为39.4 g)
C.与M的碳酸盐反应的盐酸的物质的量浓度(设为0.1 mol/L)
D.题设数据充足,不需要补充数据。
根据你的选择,计算金属M的相对原子质量为。
(3)求与滤液反应的盐酸的物质的量浓度。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com