
能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I: CO(g)+2H2(g)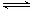 CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应II:CO2(g)+3H2(g)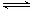 CH3OH(g)+ H2O(g) ΔH2
CH3OH(g)+ H2O(g) ΔH2
①上述反应符合“原子经济”原则的是 (填“I”或“Ⅱ”)。
②下表所列数据是反应I在不同温度下的化学平衡常数(K)。
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
由表中数据判断ΔH1 0 (填“>”、“=”或“<”)。
③某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为 ,此时的温度为
(从上表中选择)。
(2)已知在常温常压下:
① 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH =-1275.6 kJ/mol
② 2CO(g)+ O2(g)= 2CO2(g) ΔH =-566.0 kJ/mol
③ H2O(g)= H2O(l) ΔH =-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
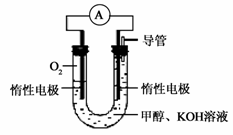 (3)某实验小组依据甲醇燃烧的反应原理,设计
(3)某实验小组依据甲醇燃烧的反应原理,设计
如右图所示的电池装置。
①该电池正极的电极反应为
。
②工作一段时间后,测得溶液的pH减小,
该电池总反应的离子方程式为
。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
A、B、C都是金属,把A浸入C的硫酸盐溶液中,A的表面有C析出,A与B和稀硫酸溶液组成原电池时,B为电池的负极。A、B、C三种金属的活动性顺序为( )
A.A>B>C B.A>C>B C.B>A>C D.B>C>A
查看答案和解析>>
科目:高中化学 来源: 题型:
有原子序数均小于20的A、B、C、D四种元素,已知:① A和B在同一主族,C和D在同一周期;② 四元素相互间可形成A2C、A2C2、B2C2、DC2等化合物;③ B的阳离子与C的阴离子核外电子层结构相同;④B2C2与A2C或DC2反应都生成C2气体;⑤ B的单质与A2C反应生成A2气体,A2与C2混合遇火可发生爆炸,生成常温下无色、无味的液体A2C.试回答:
(1)写出A和D两元素的名称:A________、D________
(2)画出B离子和C离子的结构示意图_____________ , _____________ 。
两种离子中,半径较小的是________(填离子符号)。
(3)写出A2C2、B2C2的电子式:A2C2__________ B2C2__________
(4)写出B2C2与DC2反应的化学方程式________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
下列图中的实验方案,能达到实验目的的是 ( )
| A | B | C | D | |
| 实验方案 |
|
将NO2球浸泡在冰水和热水中 |
|
|
| 实验 目的 | 验证FeCl3对H2O2分解反应有催化作用 | 探究温度对平衡 2NO2 | 除去CO2气体中混有的SO2 | 比较HCl、H2CO3和H2SiO3的酸性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
元素的性质呈周期性变化的根本原因是
A.元素的相对原子质量呈周期性变化 B.元素的原子半径呈周期性变化
C.元素的金属性和非金属性呈周期性变化 D.元素原子的核外电子排布呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述错误的是
A.13C和14C属于同一种元素,它们互为同位素
B.1H和2H是不同的核素,它们的质子数相等
C.14C和14N的质量数相等,它们的中子数不等
D.6Li和7Li的电子数相等,中子数也相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com