
| A.浓硫酸具有脱水性,因而能使蔗糖炭化 |
B.在反应HCOOH CO↑+H2O中,浓H2SO4只表现脱水性 CO↑+H2O中,浓H2SO4只表现脱水性 |
C.在反应Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O中,浓H2SO4只表现氧化性 CuSO4+SO2↑+2H2O中,浓H2SO4只表现氧化性 |
| D.浓硫酸具有吸水性,因而能使CuSO4·5H2O转化为CuSO4 |
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源:不详 题型:实验题
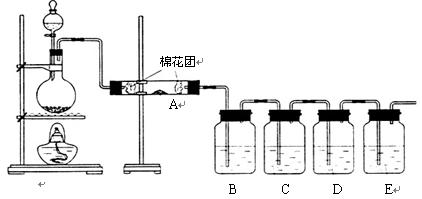
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 SO3(g);△H=" —98" kJ· mol—1。开始时在10L的密闭容器中加入4.0mol SO2(g)和5.0molO2(g),当反应达到平衡时共放出热量196kJ,该温度下平衡常数K= 。
SO3(g);△H=" —98" kJ· mol—1。开始时在10L的密闭容器中加入4.0mol SO2(g)和5.0molO2(g),当反应达到平衡时共放出热量196kJ,该温度下平衡常数K= 。 2SO3(g)达到平衡后改变下述条件SO3 的体积分数变大的是
2SO3(g)达到平衡后改变下述条件SO3 的体积分数变大的是 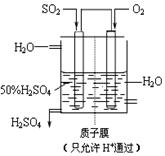
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硫酸厂应该建在靠近原料产地的地区 |
| B.接触法制硫酸的主要步骤是造气、接触氧化和三氧化硫的吸收 |
| C.由于常压下SO2转化为SO3的转化率很高,所以SO2接触氧化时不采用高压的反应条件 |
| D.工业“三废”的综合利用不仅能减少污染,还获得有用的副产品 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.二氧化硫有漂白性 | B.二氧化硫有还原性 |
| C.二氧化硫有氧化性 | D.二氧化硫溶于水后,溶液显酸性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.36.8% | B.37.6% | C.22.0% | D.无法计算 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.双氧水、臭氧都可用于杀菌消毒 | B.二氧化硫可用来漂白纸浆、毛、丝等 |
| C.浓硫酸可用于干燥NH3、H2、O2等气体 | D.红磷用于制安全火柴 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 不同质量铵盐/g | 25.00 | 50.00 | 75.00 | 100.00 |
| 浓硫酸增加的质量/g | 相同 | 相同 | 1.70 | 0 |
| A.12.15% | B.21.50% | C.14.56% | D.无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com