
 如图为向100mL 2mol/L AlCl3溶液中加入2mol/L NaOH溶液过程中,产生Al(OH)3白色沉淀的质量与NaOH的物质的量之间的关系曲线.试回答:
如图为向100mL 2mol/L AlCl3溶液中加入2mol/L NaOH溶液过程中,产生Al(OH)3白色沉淀的质量与NaOH的物质的量之间的关系曲线.试回答:分析 (1)一定量AlCl3溶液中加入NaOH溶液后,随氢氧化钠溶液的加入,先生成氢氧化铝沉淀,发生:Al3++3OH-=Al(OH)3↓,依据化学方程式的定量关系计算得到;
(2)AB段是氢氧化铝沉淀溶解的过程,反应生成偏铝酸钠和水;
(3)B处溶液为NaAlO2、NaCl,以此可判断离子的物质的量浓度;向B处生成的溶液中通入二氧化碳,可发生反应2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-;
(4)100mL2mol/L的AlCl3溶液完全反应生成氢氧化铝沉淀,应为0.2mol,即15.6g,若碱不足,只发生Al3++3OH-═Al(OH)3↓;若碱与铝离子的物质的量之比大于3:1,小于4:1,发生Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O,据此讨论计算.
解答 解:(1)由图象可知,A点是氯化铝和氢氧化钠反应生成氢氧化铝和氯化钠的反应,反应的化学方程式为:AlCl3+3NaOH=Al(OH)3↓+3NaCl,A点时已参加反应的AlCl3和NaOH的物质的量之比为1:3,
故答案为:3;
(2)AB段是氢氧化铝沉淀溶解的过程,反应生成偏铝酸钠和水,反应的离子方程式为:Al(OH)3+OH-═AlO2-+2H2O,故答案为:Al(OH)3+OH-═AlO2-+2H2O;
(3)B处溶液为NaAlO2、NaCl,可知离子的物质的量浓度最大的为Na+,向B处生成的溶液中通入二氧化碳,可发生反应2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-,反应生成白色沉淀,故答案为:Na+;生成白色沉淀;
(4)100mL2mol/L的AlCl3溶液完全反应生成氢氧化铝沉淀,应为0.2mol,即15.6g,
沉淀的质量是7.8g,其物质的量为$\frac{7.8g}{78g/mol}$=0.1mol,
①若碱不足,由Al3++3OH-═Al(OH)3↓可知,
NaOH的物质的量为0.1mol×3=0.3mol,NaOH溶液的体积为$\frac{0.3mol}{2mol/L}$=0.15L=150mL;
②碱与铝离子的物质的量之比大于3:1,小于4:1,
则由 Al3++3OH-═Al(OH)3↓
0.2mol 0.6mol 0.2mol
Al(OH)3+OH-═AlO2-+2H2O
(0.2-0.1)mol 0.1mol
则消耗的碱的物质的量为0.6mol+0.1mol=0.7mol,NaOH溶液的体积为$\frac{0.7mol}{2mol/L}$=0.35L=350mL,
答:消耗2mol/L NaOH溶液的体积可能是150mL或350mL.
点评 本题考查了铝及其化合物性质及计算,为高频考点,侧重于学生的分析能力和计算能力的考查,明确碱的量的多少对反应的影响及发生的化学反应是解答本题的关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
 大麻酚及它的衍生物都属麻醉药品,并且毒性较强.吸食大麻使人的脑功能失调、记忆力消退、健忘、注意力很难集中.吸食大麻还可破坏男女的生育能力,而且由于大麻中焦油含量高,其致癌率也较高.大麻酚分子结构如图,回答下列问题:
大麻酚及它的衍生物都属麻醉药品,并且毒性较强.吸食大麻使人的脑功能失调、记忆力消退、健忘、注意力很难集中.吸食大麻还可破坏男女的生育能力,而且由于大麻中焦油含量高,其致癌率也较高.大麻酚分子结构如图,回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
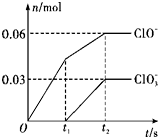 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化关系如图所示.下列说法不正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化关系如图所示.下列说法不正确的是( )| A. | Cl2和苛性钾溶液在不同温度下可能发生不同反应 | |
| B. | 反应中转移电子数为是0.42 NA | |
| C. | 原苛性钾溶液中KOH的物质的量为0.3 mol | |
| D. | 生成物中Cl-的物质的量为0.21 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 气体乙中一定含有CO2可能含有SO2 | |
| B. | 白色沉淀丁一定是AgCl | |
| C. | 固体粉末M中一定含有Cu、FeO,可能含有Fe2O3 | |
| D. | 固体乙中一定含有Fe2O3和CuO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B2A2和B2A中阴阳离子的个数比相同 | |
| B. | 原子半径的大小顺序:r(D)>r(C)>r(B)>r(A) | |
| C. | D的简单气态氢化物的热稳定性比A的强 | |
| D. | 元素C的单质是一种高硬度、高熔点的金属 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com