
【题目】I.雾霾严重影响人们的生活,汽车尾气排放是造成雾霾天气的重要原因之一。已知汽车尾气排放时容易发生以下反应:
①N2(g)+O2(g)![]() 2NO(g) △H1= a kJ·mol-1
2NO(g) △H1= a kJ·mol-1
②2NO(g)+O2(g)![]() 2NO2(g) △H2= b kJ·mol-1
2NO2(g) △H2= b kJ·mol-1
③CO(g)+1/2 O2(g)![]() CO2(g) △H3= c kJ·mol-1
CO2(g) △H3= c kJ·mol-1
④2CO(g)+2NO(g)![]() N2(g)+2CO2(g) △H4
N2(g)+2CO2(g) △H4
请回答下列问题:
(1)根据反应①②③,确定反应④中△H4= kJ·mol-1。
(2)下列情况能说明反应②已达平衡状态的是 (填编号)。
A.单位时间内生成1mol NO2的同时消耗了lmol NO
B.在恒温恒容的容器中,混合气体的密度保持不变
C.混合气体的颜色保持不变
D.在恒温恒压的容器中,NO的体积分数保持不变
II.甲醇是重要的化工原料,又可作为燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下所示:
化学反应 | 平衡 常数 | 温度/℃ | ||
500 | 700 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.34 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 1.70 | 2.52 |
③3H2(g)+CO2(g) | K3 | |||
请回答下列问题:
(1)反应②是 (填“吸热”或“放热”)反应。
(2)据反应①与②可推导出K1、K2与K3之间的关系,则K3= (用K1、K2表示)。
(3)500 ℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol·L-1)分别为0.8、0.1、0.3、0.15,则此时v正 v逆(填“>”、“=”或“<”)。
(4)反应①按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。
下列说法正确的是___________________(填序号)。
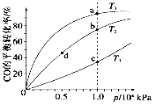
A.温度:T1>T2>T3
B.正反应速率:v(a)>v(c),v(b)>v(d)
C.平衡常数:K(a)>K(c),K(b)=K(d)
(5)新型高效的甲醇燃料电池采用铂为电极材料,两电极上分别通入CH3OH和O2。某研究小组将两个甲醇燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。回答下列问题:
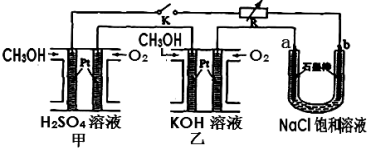
则乙燃料电池的负极反应式为 。
【答案】I.(1)2c-a (2) CD II.(1)吸热 (2)K1K2 (3)> (4)C
(5) 2CH3OH-12e-+16OH-=2CO32-+12H2O
【解析】
试题分析:I.(1)根据盖斯定律,反应②×2-③即得,确定反应④2CO(g)+2NO(g)N2(g)+2CO2(g)△H4=(2c-a)KJ/mol;
(2)A.单位时间内生成1mol NO2的同时消耗了lmol NO,都是正反应,故不能说明达到平衡状态,故A错误;B.密度=![]() ,总质量一定,体积一定,故密度一定,故混合气体的密质不再发生改变不能说明达到平衡状态,故B错误;C.因为平衡常数仅与温度有关,当平衡常数不再变化,即反应的温度不变,又在绝热恒容的容器中,所以反应的平衡常数不再变化能说明达到平衡状态,故C正确;D.在恒温恒压的容器中,NO的体积分数保持不变,则反应达平衡,能说明达到平衡状态,故D正确;故选CD。
,总质量一定,体积一定,故密度一定,故混合气体的密质不再发生改变不能说明达到平衡状态,故B错误;C.因为平衡常数仅与温度有关,当平衡常数不再变化,即反应的温度不变,又在绝热恒容的容器中,所以反应的平衡常数不再变化能说明达到平衡状态,故C正确;D.在恒温恒压的容器中,NO的体积分数保持不变,则反应达平衡,能说明达到平衡状态,故D正确;故选CD。
II.(1)反应②CO2(g)+H2(g)CO(g)+H2O(g)的平衡常数随温度升高增大,说明平衡正向进行,正反应是吸热反应;
(2)平衡常数是利用生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积,结合反应①+②得到反应③,可得平衡常数K3=K1K2;
(3)500℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为0.1molL-1、0.8molL-1、0.3molL-1、0.15molL-1,Q=![]() =0.88<K=2.5,则此时v正>v逆;
=0.88<K=2.5,则此时v正>v逆;
(4)A.根据反应①中温度与K的关系,可推断该反应为放热反应,升温,平衡左移,CO的转化率减小,所以T3>T2>T1,故A错误;B.反应速率v(c)>v(a),v(b)>v(d),故B错误;C.温度越高,平衡常数越小,压强对平衡常数无影响,所以K(a)>K(c),K(b)=K(d),故C正确;故选C。
(5)在碱性溶液中,CH3OH碱性燃料电池中,负极CH3OH失电子被氧化,反应式为:2CH3OH-12e-+16OH-=2CO32-+12H2O;


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
【题目】(一)根据要求回答下列问题:
①CaBr2 ②H2O ③NH4Cl ④H2O2 ⑤Na2O2 ⑥Ca(OH)2 ⑦HClO ⑧I2 ⑨He
(1)含有共价键的离子化合物是(用序号回答) ,含有共价键的共价化合物是(用序号回答) 。
(2)当其熔化时,不破坏化学键的是(用序号回答) 。
(二)写出下列物质或微粒的电子式:
H2O: Na2O: CO2:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D表示中学化学中的四种常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去)。

(1)若A为强碱溶液,其焰色反应显黄色,C常用作食品添加剂,请回答下列问题:
①物质的量浓度相同的B、C水溶液的pH前者 (填大于或小于)后者。
②反应Ⅲ的离子方程式是 。
③现有B和C的固体混合物ag,加热至质量不再改变时剩余固体为bg,则B的质量分数为 。
(2)若C、D均为金属单质,向A溶液中滴加硝酸银溶液,产生不溶于稀硝酸的白色沉淀,则:
①反应III的离子方程式是 。
②实验室中储存B溶液时应加入________。
③检验溶液A中金属阳离子的方法是 。
(3)若D为强电解质、B为难溶于水的沉淀,
①则A和C反应的离子方程式________________
②符合条件的D物质可能是下列物质中的________(填序号)。
a.硫酸
b.醋酸
c.氢氧化钠
d.氨水
e.氯化钡
f.硝酸镁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.化学反应除了生成新物质外,还伴随着能最的变化
B.物质燃烧和中和反应均放出热量
C.分解反应肯定是吸热反应
D.化学反应是吸热还是放热决定于生成物具有的总能最和反应物具有的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH2=CHCH2OH可能发生的反应类型有:①加成反应 ②氧化反应 ③取代反应 ④中和反应 ( )
A.只有①③ B.只有①②③ C.只有①③④ D.只有①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅的说法,不正确的是( )
A. 光导纤维的主要成分是二氧化硅
B. 二氧化硅是硅酸的酸酐,但不可以用它和水直接反应来制取硅酸
C. 硅的化学性质不活泼,但在常温下也可和某些物质反应
D. 盛放硅酸钠溶液的试剂瓶不能用玻璃塞的主要原因是硅酸钠溶液水解呈碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子中的中心原子杂化轨道的类型相同的是( )
A. SO3与SO2 B. BF3与NH3 C. BeCl2与SCl2 D. H2O与SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语正确的是
①质子数为53中子数为78的碘原子:13153I
②乙烯的结构简式CH2CH2
③硫离子结构示意图: ![]()
④过氧化氢的电子式:![]()
⑤CO2的比例模型: ![]()
⑥乙醇的结构式:CH3CH2OH
⑦丙烷分子的球棍模型: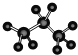
⑧T原子可以表示为31H
A.①③⑤⑥⑦⑧ B.①②③④⑦ C.①⑦⑧ D.①③⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)乙醇跟乙酸在浓硫酸存在并加热的条件下发生酯化反应(反应A),其逆反应是水解反应(反应B);反应可能经历了生成中间体(Ⅰ),过程如图所示.在A~F 6个反应中,属于加成反应的是______________(填字母)。
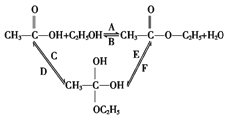
(2)按要求写出下列化学术语
ⅰ.已知在一定的条件下2CH3CH2OH→CH3CH2OCH2CH3+H2O,则类比写出CH3CH(OH)CH2CH3发生同样类型反应的化学方程式_______________________________,反应类型为_____________;
ⅱ.写出A(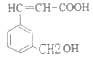 )发生下列反应的方程式:
)发生下列反应的方程式:
①A+钾→__________________________,
②A发生加聚反应__________________________;
ⅲ.已知在一定温度和压强下,1g氢气在氯气中充分燃烧生成HCl气体,放出热量为a,则在相同条件下断开1molH-H键和1molCl-Cl键所吸收的能量比形成2molH-Cl键所放出的能量______(填“多”或“少”)_______kJ。
ⅳ.用化学反应方程式表示冶炼银的反应原理__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com