
��14�֣���ͼ��ʾ�й�����֮���ת����ϵ��A��C��E��GΪ�ǽ������ʣ�����A��G�ڳ�����Ϊ���壬E�����۱�����K��һ�ֳ��õ�ʳƷ���Ӽ���L�dz�������ɫ��ζҺ�壬IΪ����ɫ���壬J����ɫ��Ӧ��dz��ɫ������ɫ�ܲ�������
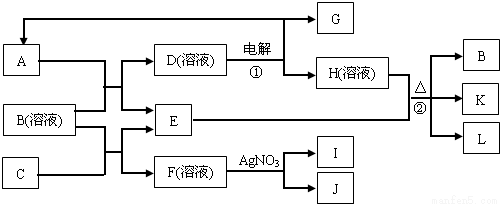
��1��B��I���������ʻ�ѧʽ�ֱ�Ϊ_______________________��
��2��д����Ӧ�ڵ����ӷ���ʽ���� _______________________��
��3��ѡ��ʵ���ұ���C���ʵ�ע������_______________��A����ɫƿ��B����ɫƿ��C��������D����������������֮���ȡ��ʲô���Ᵽ�淽����__________________________��
��4����֪A��C��E������G��Ӧ�����䷴Ӧ����Ҫ���ɸߵ���˳��Ϊ ____________���û�ѧʽ��ʾ��
��5��A��H��Һ��Ӧ������������ͻ�ԭ��������ʵ����ı�Ϊ1��1��д���˷�Ӧ�Ļ�ѧ��Ӧ����ʽ____________________��
 ѧ���쳵��������������������ϵ�д�
ѧ���쳵��������������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�갲��ʡ��һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����������Һ�����ʵ���Ũ�ȵ���0.1mol/L����
A������״����22.4LHCl�������ܽ��� 1 Lˮ��
B����10����������Ϊ98%��H2SO4��990��H2O
C����8��SO3����ˮ�����1L��Һ ����֪��SO3+H2O�TH2SO4��
D����0.1molNa2O����2 LH2O�У���֪��Na2O+H2O�T2NaOH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶�������ѡ��ѧ�Ծ��������棩 ���ͣ�ѡ����
һ���¶�ʱ����2.0 L�����ܱ������г���1.0 mol PCl5��������Ӧ��PCl5(g)?Cl2(g)
+PCl3(g)��һ��ʱ���Ӧ�ﵽƽ�⡣��Ӧ�����в�õIJ������ݼ��±���
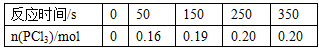
����˵����ȷ����
A����Ӧ��ǰ50 s�ڵ�ƽ������Ϊv(PCl3)=0.0032 moI��L��l��s��l
B�����������������䣬�������¶ȣ���Ӧ���´ﵽƽ�⣬ƽ��ʱc(PCl3)=0.11moI��L��l�� ������Ӧ�ġ�H<0
C����ͬ�¶��£�����ʼʱ�������г���1.0 molPCl5��0.20mol PCl3��0.20 mol Cl2����Ӧ�ﵽƽ��ǰv(��)<v(��)
D����ͬ�¶��£�����ʼʱ�������г���1.0mol PCl3��1.0 mol Cl2����Ӧ�ﵽƽ��ʱPCl3��ת����Ϊ80%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ��һ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʷ����У�ǰ�߰������ߵ���
A������������ ������ B����Һ ����
C������� ������ D������� ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶��ϵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪���з�Ӧ�������仯ʾ��ͼ���£��й�˵����ȷ����
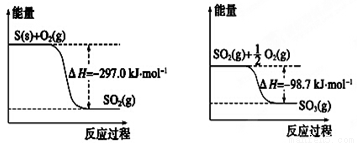
A��1 mol S��g����O2��g����ȫ��Ӧ����SO2��g������Ӧ�ų�������С��297.0 kJ
B������ͬ�����£�SO2 ��g����SO3 ��g���ȶ�
C��S(s)��O2(g)��Ӧ����SO3(g)���Ȼ�ѧ����ʽS��s����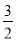 O2��g��
O2��g�� SO3��g����H����395.7kJ��mol��1
SO3��g����H����395.7kJ��mol��1
D��һ��������1 mol SO2��g����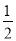 mol O2��g����Ӧ������1 mol SO3��l���ų���������98.7 kJ
mol O2��g����Ӧ������1 mol SO3��l���ų���������98.7 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�츣��ʡ�����и�����ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ�������£����������ʵ�����ϵ���з�Ӧ�����Ӧ�����ӷ���ʽ��ѧ����ʽ��д��ȷ����
A��n(Cl2)��n(Fe)��5��4 5Cl2��4Fe 2FeCl2��2FeCl3
2FeCl2��2FeCl3
B��n(Cl2)��n(FeBr2)��1��1 Fe2����2Br����Cl2=Fe3����Br2��2Cl��
C��n(MnO4��)��n(H2O2)��2��3 2MnO4����3H2O2��6H��=2Mn2����4O2����6H2O
D��n(Fe)��n[HNO3(ϡ)]��1��3 4Fe��12H����3NO3��===3Fe2����Fe3����3NO����6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�����и�����ѧ��9���ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
25��ʱ����ijһԪ��MOH��������Һ�������ϣ�����仯���Բ��ƣ�����÷�Ӧ����Һ��pH���±����������жϲ���ȷ����

A��ʵ���������Һ��c��Cl������c��M+����c��H+����c��MOH��
B����ʵ�����������Һ��ˮϡ�ͺ� ��С
��С
C��a>0.10
D��MOH�ĵ���ƽ�ⳣ�����Ա�ʾΪKb = 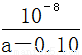
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������������ѧ������ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ˮ�������õIJ��ֹ�����ͼ��ʾ������˵���������
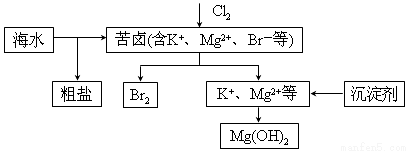
A�����±��ͨ��Cl2��Ϊ����ȡ��
B�����οɲ��ó��Ӻ��ؽᾧ�ȹ����ᴿ
C����ҵ������ѡ��NaOH��Ϊ������
D��������һ�����ÿ�����ˮ�������������壬����SO2���仹ԭ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ�߶���ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�¶������ܱ������з�����Ӧ��2M(g)+N(g) 2E(g)������ʼʱֻ����2mol E(g)���ﵽƽ��ʱ����������ѹǿ����ʼ������20%������ʼʱֻ����2mol M��1mol N�Ļ������ﵽƽ��ʱM��ת����Ϊ
2E(g)������ʼʱֻ����2mol E(g)���ﵽƽ��ʱ����������ѹǿ����ʼ������20%������ʼʱֻ����2mol M��1mol N�Ļ������ﵽƽ��ʱM��ת����Ϊ
A��80% B��60% C��40% D��20%
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com