
| A.最外层有8个电子的原子 |
| B.最外层电子排布为ns2的原子 |
| C.次外层无未成对电子的原子 |
| D.最外层有3个未成对电子的原子 |
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X原子的电子层数比Y的多 |
| B.X的最高价含氧酸的酸性比Y的弱 |
| C.X的气态氢化物比Y的稳定 |
| D.Y的单质能将X从NaX的溶液中置换出来 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.N:1s22s22p3 | B.S2-:1s22s22p63s23p6 |
| C.Na:1s22s22p53s2 | D.Si:1s22s22p63s23p2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
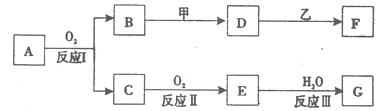
 ;D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。则:
;D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。则:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com