
| A. | 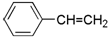 | B. | 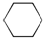 | C. | 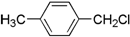 | D. | 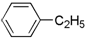 |
分析 同系物指结构相似,在分子组成上相差一个或若干个CH2原子团的物质,具有如下特征:结构相似、化学性质相似、分子式通式相同,分子式不同、物理性质不同,研究范围为有机物.
芳香烃通常指分子中含有苯环结构的碳氢化合物;苯的同系物含有1个苯环,侧链为烷基,组成通式为CnH2n-6.
解答 解:A. 是含有苯环结构的碳氢化合物,属于芳香烃,侧链是乙烯基,含有双键,不是烷基,不是苯的同系物,故A错误;
是含有苯环结构的碳氢化合物,属于芳香烃,侧链是乙烯基,含有双键,不是烷基,不是苯的同系物,故A错误;
B. 不含苯环,不是苯的同系物,故B错误;
不含苯环,不是苯的同系物,故B错误;
C. 含有卤素原子:Cl,不属于芳香烃,属于烃的衍生物,故C错误;
含有卤素原子:Cl,不属于芳香烃,属于烃的衍生物,故C错误;
D. 是含有苯环结构的碳氢化合物,属于芳香烃,侧链是乙基,分子组成比苯多2个CH2原子团,是苯的同系物,故D正确;
是含有苯环结构的碳氢化合物,属于芳香烃,侧链是乙基,分子组成比苯多2个CH2原子团,是苯的同系物,故D正确;
故选D.
点评 本题以有机物的结构为载体考查芳香烃、苯的同系物、难度不大,注意有机化学“五同”理解辨析与芳香烃概念、苯的同系物结构特点.


科目:高中化学 来源: 题型:选择题
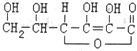 ,有关它的叙述不正确的是( )
,有关它的叙述不正确的是( )| A. | 在碱性溶液中能稳定存在 | |
| B. | 容易发生氧化反应和加成反应 | |
| C. | 可以溶解于水,溶液显酸性 | |
| D. | 可以看作环状酯类化合物,分子式为C6H8O6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na和O2 | B. | Fe和FeCl3 | C. | Na2CO3和HCl | D. | AlCl3和NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 H、C、N、O、Al、S是常见的六种元素.
H、C、N、O、Al、S是常见的六种元素.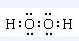 或H:C??C:H.
或H:C??C:H.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置.其材料除单晶硅,还有铜铟镓硒等化合物.
太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置.其材料除单晶硅,还有铜铟镓硒等化合物.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
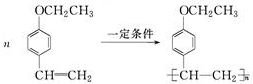
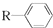 $→_{一定条件}^{CO、HCl}$
$→_{一定条件}^{CO、HCl}$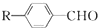 ,为合成某种液晶材料的中间体M,有人提出如下不同的合成途径:
,为合成某种液晶材料的中间体M,有人提出如下不同的合成途径: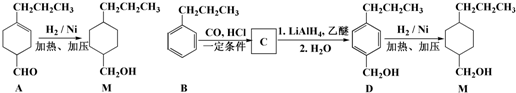
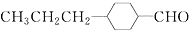 和
和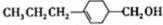 (写结构简式)生成.
(写结构简式)生成.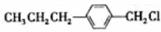 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
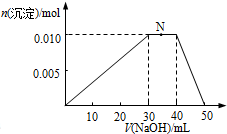
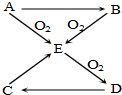 已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素.
已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com